ポイント
- 肝がんでヒストンH4K5のラクチル化が特異的に亢進し、悪性度および予後と有意に関連する新規バイオマーカーであることを発見。
- H4K5ラクチル化が解糖系酵素ENO2の発現を高め、乳酸産生を介した「正のフィードバックループ」により肝がんの悪性化を促進する分子機構を解明。
- ENO2阻害によりH4K5ラクチル化と腫瘍増殖が抑制され、H4K5ラクチル化–ENO2経路が新たな治療標的となる可能性を提示。
概要
東京科学大学(Science Tokyo) 医歯学総合研究科 分子腫瘍医学分野の田中真二教授、秋山好光講師、島田周助教、波多野恵助教、山根聖弘大学院生らの研究チームは、同大学の肝胆膵外科および人体病理学分野と共同で、肝がんにおける新規ヒストン修飾[用語1]機構としてのヒストンラクチル化[用語2]の役割と、その分子制御機構を解明しました。
本研究の結果、肝がんではヒストンH4K5(ヒストンH4の5番目のリジン)のラクチル化が腫瘍部で特異的に高く、予後を予測する新規バイオマーカーであることが示されました。さらに、H4K5ラクチル化がヒストン修飾酵素EP300[用語3]によって形成されることを明らかにしました。また、H4K5ラクチル化の増加は、解糖系[用語4]酵素エノラーゼ2(ENO2)[用語5]の発現を高め、ENO2による解糖系の亢進によって細胞内乳酸濃度が上昇し、その乳酸が再びH4K5ラクチル化を促進するという「正のフィードバックループ」を発見しました。さらに、ENO2の阻害がこのループを遮断し、腫瘍増殖を有意に抑制することを確認しました。
本研究は、解糖系とエピゲノム[用語6]異常が肝がんの悪性化を促進するメカニズムを解明するとともに、H4K5ラクチル化-ENO2ループが有望な治療標的となる可能性を示しました。
本成果は、2月17日付(現地時間)の欧州肝臓学会誌「JHEP Reports 」にオンライン掲載されました。
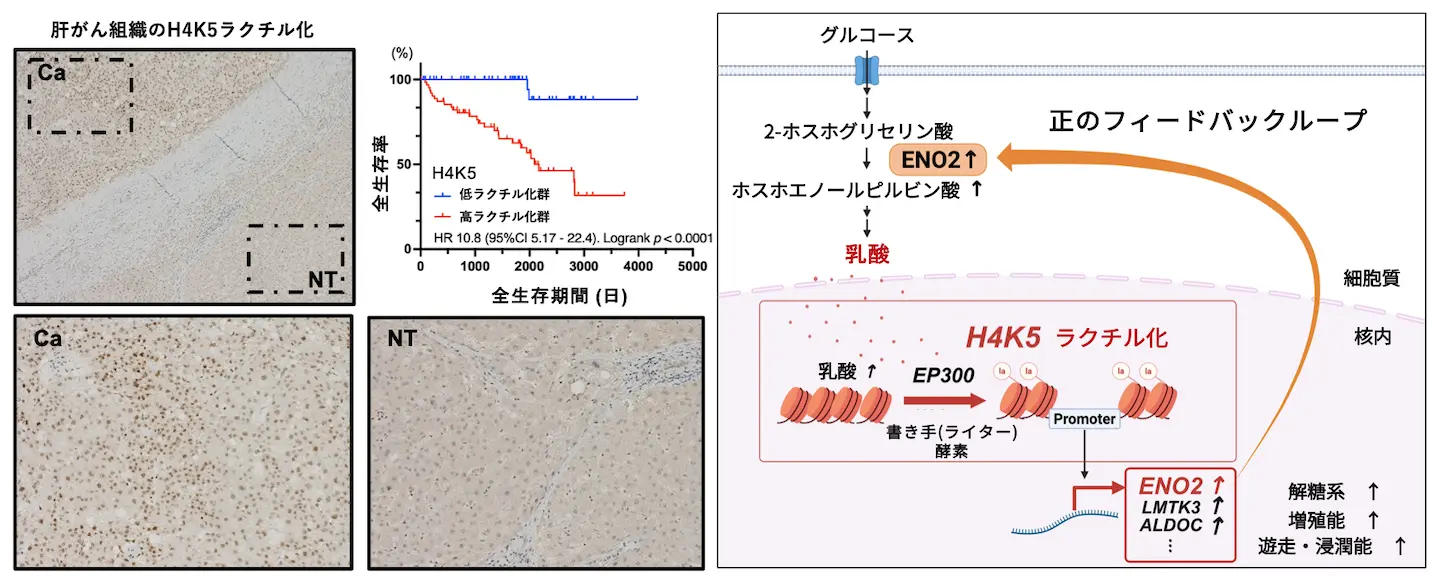
H4K5ラクチル化はがん部(Ca)の方が非腫瘍部(NT)よりも強く、亢進群は予後不良と関連していた。またH4K5ラクチル化とENO2は正のフィードバックループを形成することで、解糖系を亢進させ、肝がんの増殖と進行を促進することが示唆された。
背景
がん細胞は、酸素が存在する条件下でも解糖系を優先的に利用する代謝特性を示し(Warburg効果[用語7])、その結果、がん細胞内および周囲の微小環境には、解糖系の最終代謝産物である乳酸が大量に蓄積します。近年、この乳酸がヒストンタンパク質のリジン残基に付加される新規エピゲノム修飾「ヒストンラクチル化」の供与体として機能することが明らかになりました。ヒストンラクチル化の異常は、悪性腫瘍を含む多くの疾患において注目を集めています。
ラクチル化は、主にヒストンH3およびH4の特定のリジン残基に生じる修飾が代表的です。特に、ヒストンH3K18(18番目のリジン)のラクチル化の亢進は、肝がんを含む多くのがんにおいて腫瘍促進的に働くことが知られています。しかしながら、ヒストンH4のラクチル化に関する報告は限られており、H4ラクチル化の肝がんにおける臨床的意義や機能的役割については、これまで十分に解明されていませんでした。
研究成果
肝がん切除検体104例を対象とした免疫組織化学染色により、H4K5ラクチル化は、非腫瘍部の肝組織と比較して、がん部で特異的に亢進していることが明らかになりました(図1)。H4K5ラクチル化の亢進例は腫瘍径が大きく、臨床病理学的にも悪性度が高い特徴を示し、全生存期間および無再発生存期間が有意に短縮していました。これらの結果から、H4K5ラクチル化亢進は、肝がん患者の予後を予測する新規バイオマーカーとなる可能性が示されました(図1)。
H4K5ラクチル化の分子機構解析により、肝がん細胞ではヒストンアセチル化修飾酵素EP300が、H4K5をラクチル化する「書き手(ライター)」酵素として機能することを解明しました。さらに、H4K5ラクチル化の標的遺伝子として、解糖系酵素の一つであるENO2をはじめ、がん促進機能を有するLMTK3、ALDOC、KANK3など複数の遺伝子を同定しました。
次に、肝がん細胞においてENO2を過剰発現させると、細胞内のホスホエノールピルビン酸、ピルビン酸および乳酸の濃度が上昇し、それに伴ってH4K5ラクチル化レベルも亢進しました。一方、ENO2をノックダウンすると、これらの代謝産物およびH4K5ラクチル化は低下しました。また、ENO2ノックダウン細胞においてENO2を再発現させると、H4K5ラクチル化レベルは回復しました。これらの結果から、H4K5ラクチル化の亢進がENO2発現を増強し、ENO2が解糖系を亢進させることで乳酸産生を促進し、その乳酸が再びH4K5ラクチル化を促進するという「正のフィードバックループ」の存在が明らかとなりました。さらに、H4K5ラクチル化–ENO2ループが肝がんの悪性化を促進することが示唆されました(図1)。
マウス皮下移植モデルを用いた実験では、ENO2ノックダウン細胞の腫瘍形成能は著しく低下し、腫瘍組織内のH4K5ラクチル化レベルも低下しました。一方、ENO2を高発現させた肝がん細胞を有するマウス腫瘍モデルでは、腫瘍増殖能およびH4K5ラクチル化が増加しましたが、ENO2活性阻害剤の投与群では、体重減少などの明らかな全身毒性を認めることなく、腫瘍増殖の抑制とH4K5ラクチル化レベルの低下が認められました(図2)。これらの結果は、H4K5ラクチル化-ENO2経路の遮断が、肝がんに対する有効な治療戦略となり得ることを示しています。
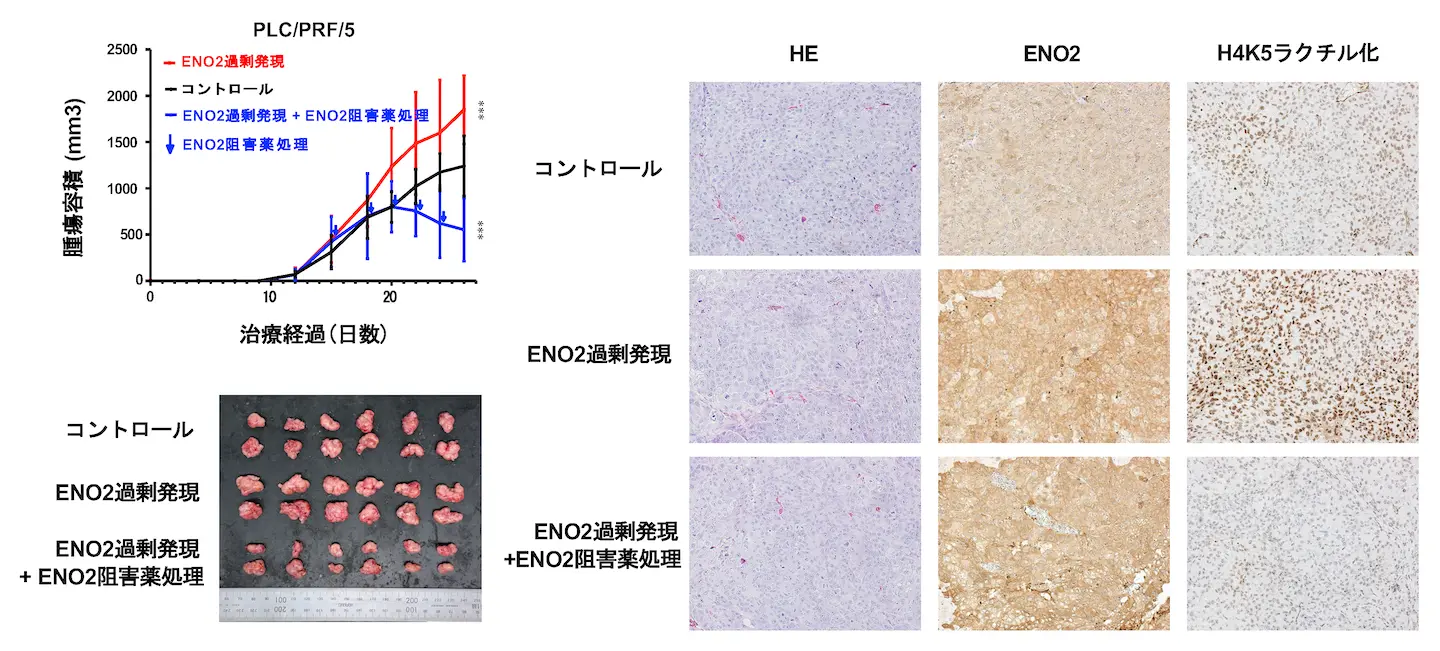
ENO2活性阻害剤処理によって腫瘍増殖は抑制した。移植腫瘍ではENO2発現に変化はなかったが、活性が阻害されることでH4K5ラクチル化は低下した。
社会的インパクト
本研究により、ヒストン修飾であるH4K5ラクチル化が、肝がんの悪性度および予後を反映する新規バイオマーカーとして有効であることが示されました。本修飾を指標とすることで、術後の予後予測や治療方針の決定に役立つ可能性が示唆されました。
また、解糖系とエピジェネティクスをつなぐH4K5ラクチル化-ENO2ループという新たな分子経路の発見は、従来の治療法に抵抗性を示す難治性肝がんに対し、代謝阻害とエピジェネティクス制御を組み合わせた新規治療法の開発につながる基盤となることが期待されます。
今後の展開
研究ではENO2阻害剤の有効性が示されました。しかし、臨床応用に向けては、赤血球へのオフターゲット効果などの副作用を回避するため、標的特異性の向上やドラッグデリバリーシステムの改良が必要です。
また、EP300を標的としたヒストンアセチル化酵素(HAT)阻害剤をはじめ、さまざまなエピゲノム治療薬の開発が現在進められています。今後は、ENO2阻害剤とエピゲノム治療薬との併用における有効性および安全性の検証が重要であると考えられます。
付記
本研究は日本学術振興会(JSPS)科学研究費助成事業(JP19H01055、JP23H02979、JP23K27670、JP24K02320、JP22K19554、JP25K22639、JP25K22573)、国立研究開発法人日本医療研究開発機構(AMED)「肝炎等克服実用化研究事業」および「次世代がん医療創生研究事業」、高松宮妃癌研究基金研究助成金などのもとに行われたものです。
用語説明
- [用語1]
- ヒストン修飾:ヒストンタンパク質の特定のアミノ酸残基(リジンやアルギニンが代表的)で認められるメチル化、アセチル化、ラクチル化などの化学修飾。これらの修飾はライター(書き込み酵素)、リーダー(読み取りタンパク質)、イレーサー(消去酵素)によって制御されている。
- [用語2]
- ヒストンラクチル化:DNAが巻き付いているヒストンタンパク質に、乳酸由来のラクチル基が付加される翻訳後修飾。遺伝子発現の活性化に関わるヒストン修飾として2019年に発見された。
- [用語3]
- EP300(E1A binding protein p300):ヒストンアセチル化を触媒する代表的な酵素としてられるが、ヒストンラクチル化酵素としても機能する。
- [用語4]
- 解糖系:グルコース(ブドウ糖)をピルビン酸や乳酸に分解してエネルギーを得る代謝経路。
- [用語5]
- エノラーゼ2(ENO2):解糖系の主要な酵素の一つで、2-ホスホグリセリン酸をホスホエノールピルビン酸に変換する反応を触媒する。神経特異的エノラーゼ(NSE)としても知られるが、脳腫瘍、肺がん、大腸がん、膵がん、肝がんなど特定のがんで高発現が報告されている。
- [用語6]
- エピゲノム:DNAの塩基配列の変化を伴わずに、遺伝子の発現を制御するDNAのメチル化やヒストン修飾などの総体。
- [用語7]
- Warburg効果:がん細胞が酸素の有無にかかわらず、エネルギー効率の良い酸化的リン酸化よりも、効率の悪い解糖系を優先的に利用してエネルギー(ATP)を産生する現象。これにより乳酸が大量に産生される。
論文情報
- 掲載誌:
- JHEP Reports
- タイトル:
- H4K5 Lactylation - ENO2 Loop Drives Glycolysis and HCC Progression
- 著者:
- Masahiro Yamane, Yoshimitsu Akiyama, Shu Shimada, Shuichi Watanabe, Megumi Hatano, Shu Tsukihara, Suguru Miyazawa, Hanako Tamura, Atsushi Nara, Keita Kodera, Kohei Okazaki, Yoshiaki Tanji, Yosuke Igarashi, Atsushi Kamachi, Kentaro Umemura, Koya Yasukawa, Keiichi Akahoshi, Kenichi Ohashi, Daisuke Ban, Shinji Tanaka
研究者プロフィール
田中 真二 Shinji Tanaka
東京科学大学 医歯学総合研究科 分子腫瘍医学分野 教授
研究領域:分子腫瘍医学、消化器外科学
秋山 好光 Yoshimitsu Akiyama
東京科学大学 医歯学総合研究科 分子腫瘍医学分野 講師
研究領域:分子腫瘍医学
山根 聖弘 Masahiro Yamane
東京科学大学 医歯学総合研究科 肝胆膵外科分野 大学院生
研究領域:分子腫瘍医学、肝胆膵外科学