ポイント
- サイトカイン誘導性mRNA医薬を腫瘍内に投与し、抗癌剤・免疫チェックポイント阻害剤を併用することで、膵癌の腹膜播種を含む腫瘍増殖を抑制し、生命予後を有意に延長した。
- 本治療法(MIMIC)は、樹状細胞とT細胞を増加・活性化させ、低下していた癌免疫反応を効果的に回復させることを明らかにした。
- 本研究は、治療選択肢が限られていた膵癌腹膜播種に対する新たな免疫治療戦略として、MIMICの有効性を示した。
概要
東京科学大学(Science Tokyo)大学院医歯学総合研究科 分子腫瘍医学分野の田中真二教授、島田周助教、丹治芳明連携研究員、ならびに総合研究院 難治疾患研究所 先端ナノ医工学分野の内田智士教授らの研究グループは、同大学肝胆膵外科分野および東京慈恵会医科大学 外科学講座との共同研究において、以下の成果を明らかにしました。
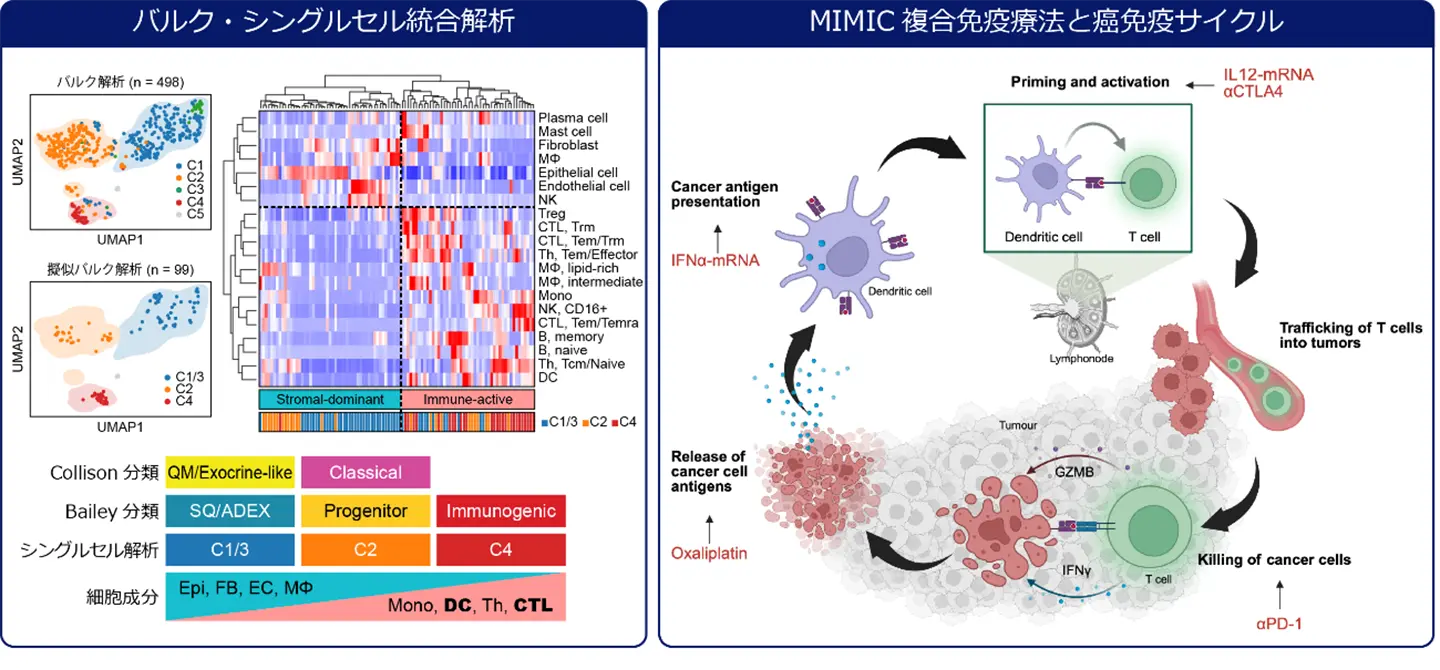
研究グループは、膵癌臨床検体を用いたバルク・シングルセル解析[用語1]および免疫組織染色解析により、予後不良膵癌では樹状細胞[用語2]とT細胞[用語3]が枯渇し、免疫活性が低い、いわゆる「冷たい腫瘍」となっていることを明らかにしました(図1左)。
さらに、腹膜播種と皮下腫瘍を同時に形成する膵癌マウスモデルを作製し、樹状細胞を活性化させるIFNαおよびT細胞を活性化させるIL12という2種類のサイトカイン[用語4]を発現するmRNA医薬[用語5]を皮下腫瘍内に直接投与しました。これに抗癌剤オキサリプラチンおよび免疫チェックポイント阻害剤[用語6]である抗PD-1抗体、抗CTLA-4抗体を併用した複合免疫療法(MIMIC)の有効性を検討しました。
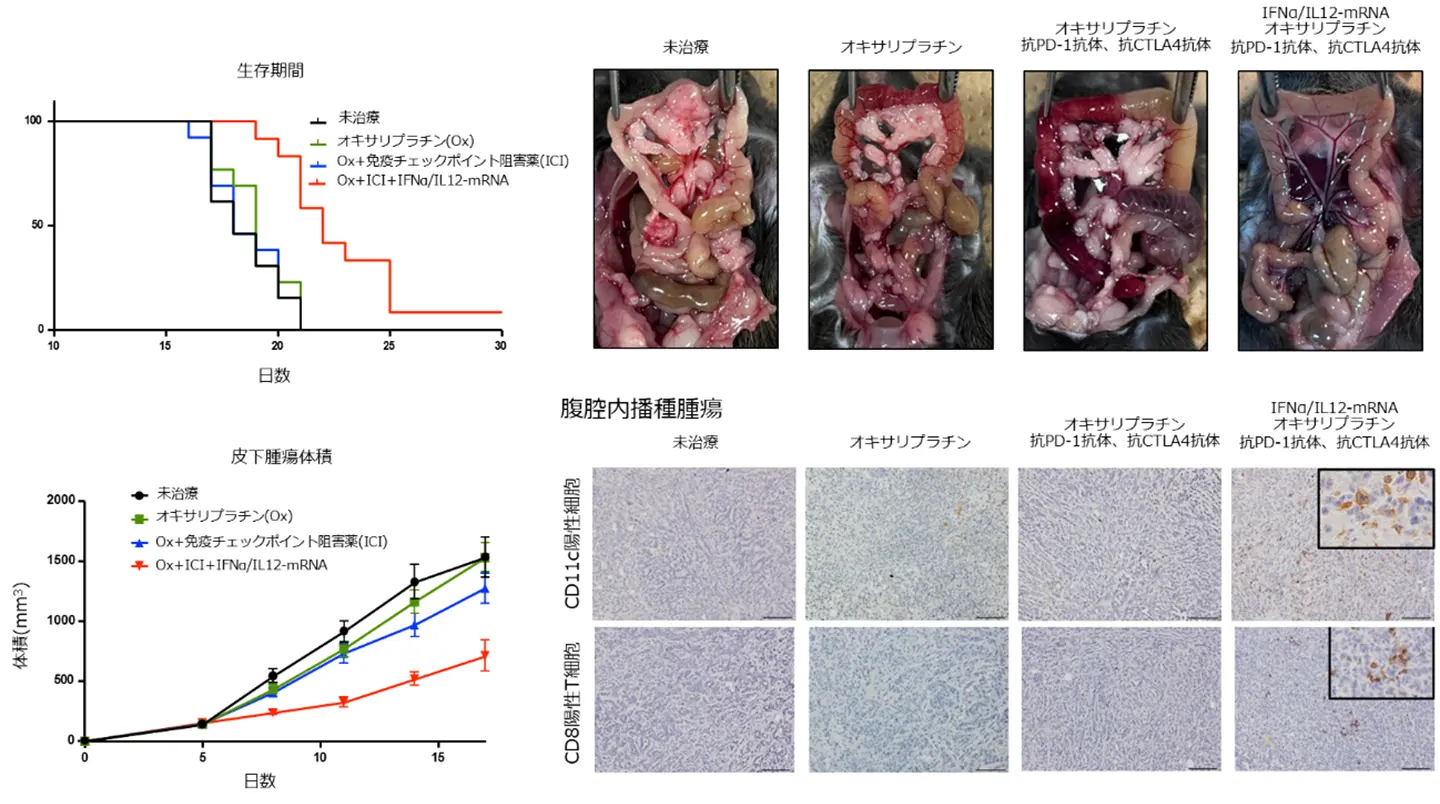
その結果、投与腫瘍において増殖抑制ならびに樹状細胞およびT細胞の増加・活性化が認められただけでなく、腹膜播種に対しても同様の効果が得られ、有意な生命予後の延長が確認されました(図1右)。
本研究で示したサイトカイン誘導性mRNAを用いた医薬複合免疫療法MIMICは、QOLを著しく損ない、抗癌剤や免疫チェックポイント阻害剤の有効性が乏しい膵癌腹膜播種という予後不良疾患に対し、画期的な治療方法となる可能性があります。
本成果は、2月3日付(現地時間)の「EBioMedicine 」誌に掲載されました。
背景
膵癌は極めて致死率の高い悪性腫瘍であり、手術、化学療法、放射線療法、免疫療法などの集学的治療が進歩しているにもかかわらず、5年生存率は約10%と依然として低く、極めて予後不良な疾患です。また、腹膜播種は膵癌の25~50%に発症し、腹部膨満や疼痛といった重篤な症状を引き起こすことで、患者のQOL(生活の質)を著しく損ないます。化学療法による延命効果は限定的であり、免疫チェックポイント阻害薬との併用についても追加的な臨床効果は乏しく、次世代免疫療法においても、大規模臨床試験で有意な予後延長効果を示せていないのが現状です。
本研究では、腹膜播種を伴う予後不良膵癌を対象に、臨床検体を用いて治療抵抗性の原因を究明しました。その上で、従来の免疫チェックポイント阻害剤に代表される「免疫抑制を解除する治療」にとどまらず、「免疫を局所的かつ直接的に活性化する治療」としてサイトカイン誘導性mRNA医薬を採用し、新たな治療戦略の検討を行いました。
研究成果
本研究では、膵癌臨床検体について498症例のバルクRNA-seqデータ と99症例のシングルセルRNA-seqデータを統合解析しました。その結果、膵癌は、線維芽細胞や血管内皮細胞などの間質成分が多いstromal-dominantサブタイプと樹状細胞やT細胞などの免疫細胞成分が多いimmune-activeサブタイプに分類されることが明らかになりました(図1左)。実際に、本学肝胆膵外科で手術切除された膵癌臨床検体112症例を用いた免疫組織染色解析において、樹状細胞やT細胞の浸潤が少ない、いわゆる「冷たい腫瘍」は有意に予後不良であることが示され、膵癌治療においては免疫抑制性の腫瘍微小環境を改善することが重要であると考えられました。
次に、膵癌で高頻度に認められるKRASおよびp53に変異を有するマウス膵癌細胞株FC1245を用い、原発腫瘍に見立てた皮下腫瘍と腹膜播種を同時に形成するマウスモデルを作製しました。このマウスモデルの腫瘍は、樹状細胞およびT細胞の浸潤が極めて少ない「冷たい腫瘍」を呈しており、従来の抗癌剤、免疫チェックポイント阻害剤、ならびにそれらの併用療法に対して治療抵抗性を示すことを確認しました。
免疫抑制性の腫瘍微小環境を改善する鍵として、癌免疫サイクル、すなわち
- 癌抗原の放出
- 樹状細胞による抗原提示
- T細胞の活性化
- T細胞の移動および腫瘍内浸潤
- 癌細胞の認識と攻撃
という一連の免疫反応に着目しました(図1右)。膵癌の治療抵抗性は、癌免疫サイクルのいずれかの段階に異常が生じ、十分に駆動されていないことが原因であると考え、抗癌剤オキサリプラチン(1.)、抗PD-1抗体(5.)、抗CTLA-4抗体(3.)に加え、樹状細胞を活性化させるIFNα(2.)およびT細胞を活性化させるIL12(3.)という2種類のサイトカインを併用投与することを検討しました。IFNαおよびIL12はいずれも全身投与では副作用が強いことが報告されているため、本学先端ナノ医工分野の内田智士教授の協力のもと、これらをコードするmRNA医薬を腫瘍内に局所投与する方法を採用しました。
その結果、5剤併用群では、mRNA医薬を局所投与した皮下腫瘍において腫瘍増殖の抑制と、樹状細胞およびT細胞の増加・活性化が認められました。さらに、活性化された免疫応答は腹膜播種にも及び、腹膜播種の個数、総体積、総重量はいずれも減少し、担癌マウスの予後を有意に延長しました(図2)。このように、局所治療によって誘導された免疫応答が、直接治療していない遠隔病変にも波及して抗腫瘍効果を示す現象は「アブスコーパル効果[用語7]」として知られており、微小転移や肉眼的に確認できない癌細胞を含む全身病変を制御できる免疫応答メカニズムとして注目されています。
また、5剤併用群は他群と比較して、免疫原性細胞死[用語8]を強力に誘導し、腫瘍内に浸潤する樹状細胞およびT細胞を増加・活性化させることで、癌免疫サイクルを効率的に駆動することが明らかにしました。さらに、5剤併用療法から1剤でも欠落すると治療効果が失われることを検証し、本併用療法が腹膜播種を伴う予後不良膵癌に対して有効であることを実証しました。
社会的インパクト
抗癌剤や免疫チェックポイント阻害剤に対して治療抵抗性を示す「冷たい腫瘍」の代表格である膵癌、特に予後不良の原因となる腹膜播種に対し、「免疫を局所的かつ直接的に活性化する治療」としてサイトカイン誘導性mRNA医薬を併用することで、予後を大きく改善することができる可能性が示唆されました。
新型コロナウイルスに対するmRNAワクチンの実用化を背景として、mRNA医薬の大量製造、安全性評価、品質管理に関する産業基盤はすでに確立されており、サイトカイン誘導性mRNA医薬の早期臨床応用が期待されます。
膵癌診療では、上部消化管内視鏡下に経胃的に膵腫瘍を採取して組織型を診断するほか、術前に審査腹腔鏡を用いて腹膜播種の有無を精査します。このような現在の膵癌診療の枠組みを応用することで、サイトカイン誘導性mRNA医薬を腫瘍に局所投与することは十分実現可能であり、技術的な観点からも早期の臨床応用が見込まれます。
今後の展開
我々は、サイトカイン誘導性mRNA医薬を中心とする複合免疫療法を、正常な癌免疫サイクルを模倣するという意味も込めて、MIMIC(Multimodal Immunotherapies with mRNA-Induced Cytokines)と名付けました。本研究では、最も予後が悪く免疫療法が奏効しにくい膵癌腹膜播種を対象に、MIMICの有効性を検討しました。
今後は、腹膜播種を伴うスキルス胃癌や肝細胞癌など、他の難治性癌についても、
- 各腫瘍の免疫プロファイルを解析する
- その免疫プロファイルを再現したマウスモデルを作製する
- 癌免疫サイクルのどの段階に異常があり、どの段階に介入すべきかを同定する
-
抗癌剤、分子標的治療薬、免疫チェックポイント阻害剤、サイトカイン誘導性mRNA医薬を組み合わせて有効性を検討する
という一連の手順により、MIMICの開発および最適化を進めていきます。
付記
本研究は文部科学省科学研究費補助金(19H01055, 23K27670, 24K02320, 22K08864, 25K11997, 20K21627, 22K19554)、国立研究開発法人日本医療研究開発機構(AMED)「肝炎等克服実用化研究事業」および「次世代がん医療創生研究事業」、高松宮妃癌研究基金研究助成金などのもとにおこなわれたものです。
用語説明
- [用語1]
- バルク・シングルセル解析:バルク解析は腫瘍組織全体の遺伝子発現を、シングルセル解析は細胞ごとの遺伝子発現を網羅的に解析する手法。
- [用語2]
- 樹状細胞:癌細胞由来の抗原を提示し、T細胞を活性化させる免疫細胞。
- [用語3]
- T細胞:樹状細胞に提示された癌抗原を認識・記憶し、癌細胞を攻撃する免疫細胞。
- [用語4]
- サイトカイン:免疫細胞の働きを調節する情報伝達物質。
- [用語5]
- mRNA医薬:タンパク質合成の鋳型となるmRNAを脂質ナノ粒子に封入した医薬品。SARS-CoV-2に対するmRNワクチンと同様の技術が用いられている。
- [用語6]
- 免疫チェックポイント阻害剤:免疫細胞の働きを抑制する免疫チェックポイント分子を阻害する薬剤。近年、さまざまな悪性腫瘍に対する有効性が報告されている。
- [用語7]
- アブスコーパル効果:局所治療部位(=scope)から外れた遠隔腫瘍(ab=離れた)にも抗腫瘍効果が波及する現象で、放射線治療において最初に報告された。
- [用語8]
- 免疫原性細胞死:癌細胞が死滅する際に、DAMPsと呼ばれる免疫活性物質を放出する現象。
論文情報
- 掲載誌:
- EBioMedicine
- タイトル:
- Cytokine mRNA-based therapy alleviates dendritic cell and T cell paucity to eliminate aggressive pancreatic cancer in preclinical mouse models
- 著者:
- Yoshiaki Tanji, Shu Shimada, Megumi Kato, Yoshimitsu Akiyama, Megumi Hatano, Shu Tsukihara, Yosuke Igarashi, Keita Kodera, Kohei Okazaki, Koya Yasukawa, Kentaro Umemura, Atsushi Kamachi, Atsushi Nara, Masahiro Yamane, Yoshiya Ishikawa, Erika Mochizuki, Yuki Mochida, Toru Ikegami, Daisuke Ban, Satoshi Uchida, Shinji Tanaka
研究者プロフィール
田中 真二 Shinji Tanaka
東京科学大学 大学院医歯学総合研究科 分子腫瘍医学分野 教授
研究領域:分子腫瘍医学、消化器外科学
島田 周 Shu Shimada
東京科学大学 大学院医歯学総合研究科 分子腫瘍医学分野 助教
研究領域:分子腫瘍医学
丹治 芳明 Yoshiaki Tanji
東京科学大学 大学院医歯学総合研究科 分子腫瘍医学分野 連携研究員
研究領域:分子腫瘍医学、肝胆膵外科学
内田 智士 Satoshi Uchida
東京科学大学 総合研究院難治疾患研究所 先端ナノ医工学分野 教授
研究領域:核酸医薬、薬物送達システム、遺伝子治療、生体材料
関連リンク
東京科学大学 大学院医歯学総合研究科 分子腫瘍医学分野
助教 島田 周
- shimada@tmd.ac.jp