ポイント
- 薬物送達システム(DDS)で広く用いられるポリエチレングリコール(PEG)と、体内で産生される抗PEG抗体が結合する強さと距離を1分子レベルで測定。
- PEGの末端基(メトキシ基またはヒドロキシ基)とその水和構造の違いが抗体との結合力を決めることを発見。
- 免疫系によって排除されにくい、より長寿命で安全なDDS製剤(ナノメディシン)の設計への新たな指針として期待。
概要
東京科学大学(Science Tokyo) 物質理工学院 材料系の林智広准教授とグレン・ビレナ・ラターク(Glenn Villena Latag)大学院生(博士後期課程)、九州大学 大学院工学研究院の森健教授らの研究チームは、薬物送達システム(DDS)のコーティング剤として広く利用されているポリエチレングリコール(PEG)[用語1]と、それに対する抗体(抗PEG抗体)との相互作用メカニズムを1分子レベルで解明しました。
コロナウィルスワクチンに代表されるように、PEGは薬剤を免疫系から隠す「ステルス高分子」として利用されていますが、近年、PEGに対する抗体が体内で作られ、薬効の低下やアレルギー様反応を引き起こすことが問題となっています。
研究チームは原子間力顕微鏡(AFM)[用語2]を用いた単一分子力学測定により、抗PEG抗体がPEG鎖を認識して結合・解離する際の微小な力を直接測定しました。その結果、現在医薬品に多く使われている、末端がメトキシ基のPEG(m-PEG)に比べ、末端がヒドロキシ基のPEG(HO-PEG)では、抗体の結合力が弱まることを発見しました。さらに、水晶振動子マイクロバランス(QCM-D)[用語3]やフーリエ変換赤外分光法(FT-IR)[用語4]を用いた解析により、HO-PEGは表面に厚い水和層(水のバリア)を形成しており、これが抗体のアクセスを妨げていることを明らかにしました。
この成果は、抗PEG抗体による免疫認識を防ぐ可能性を示すものであり、より副作用が少なく、薬効が持続する次世代のナノメディシン開発への貢献が期待されます。
本成果は、1月20日付(現地時間)の「ACS Applied Bio Materials」誌に掲載されました。
背景
がん治療やワクチンなどの薬物送達システム(DDS)製剤では、薬物を内包したナノ粒子表面をポリエチレングリコール(PEG)で覆うことで、異物として免疫細胞に認識されるのを防ぎ、血中滞留性を向上させる「PEG化」が標準的な技術として用いられています。PEGは長らく免疫原性がない(抗体を作らせない)と考えられてきましたが、近年、PEG化製剤の投与により「抗PEG抗体」が誘導されることや、既存の抗体を持つ患者において薬剤が急速に分解・排出される現象(ABC現象)が報告され、臨床上の大きな問題となっています。しかしこれまでは、抗PEG抗体がどのようにPEGを認識しているのか、特にPEGの末端構造の違いが結合にどう影響するのかについて、分子レベルでの詳細なメカニズムは不明のままでした。
研究成果
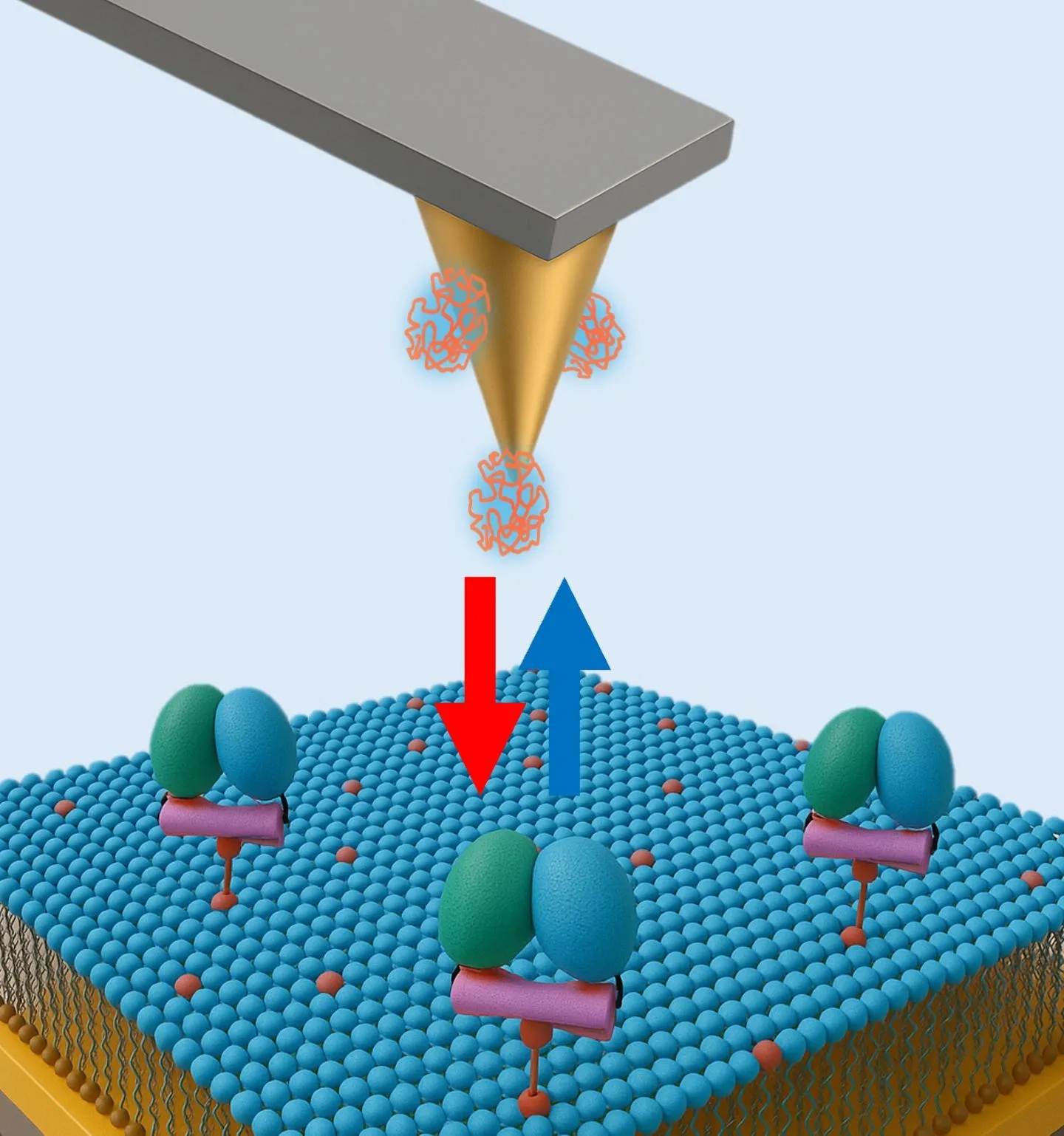
研究チームは、AFMの探針(プローブ)にPEG分子を、基板側に抗PEG抗体を固定し、両者の間に働く結合力を1分子レベルで測定しました。この抗PEG抗体としては、DDS製剤投与により生じる「ナイーブ抗体」と、親和性が高まった「成熟抗体」の2種を用意しました。その結果、以下の事実が明らかになりました。
-
成熟抗体は強く、ナイーブ抗体は弱く結合する
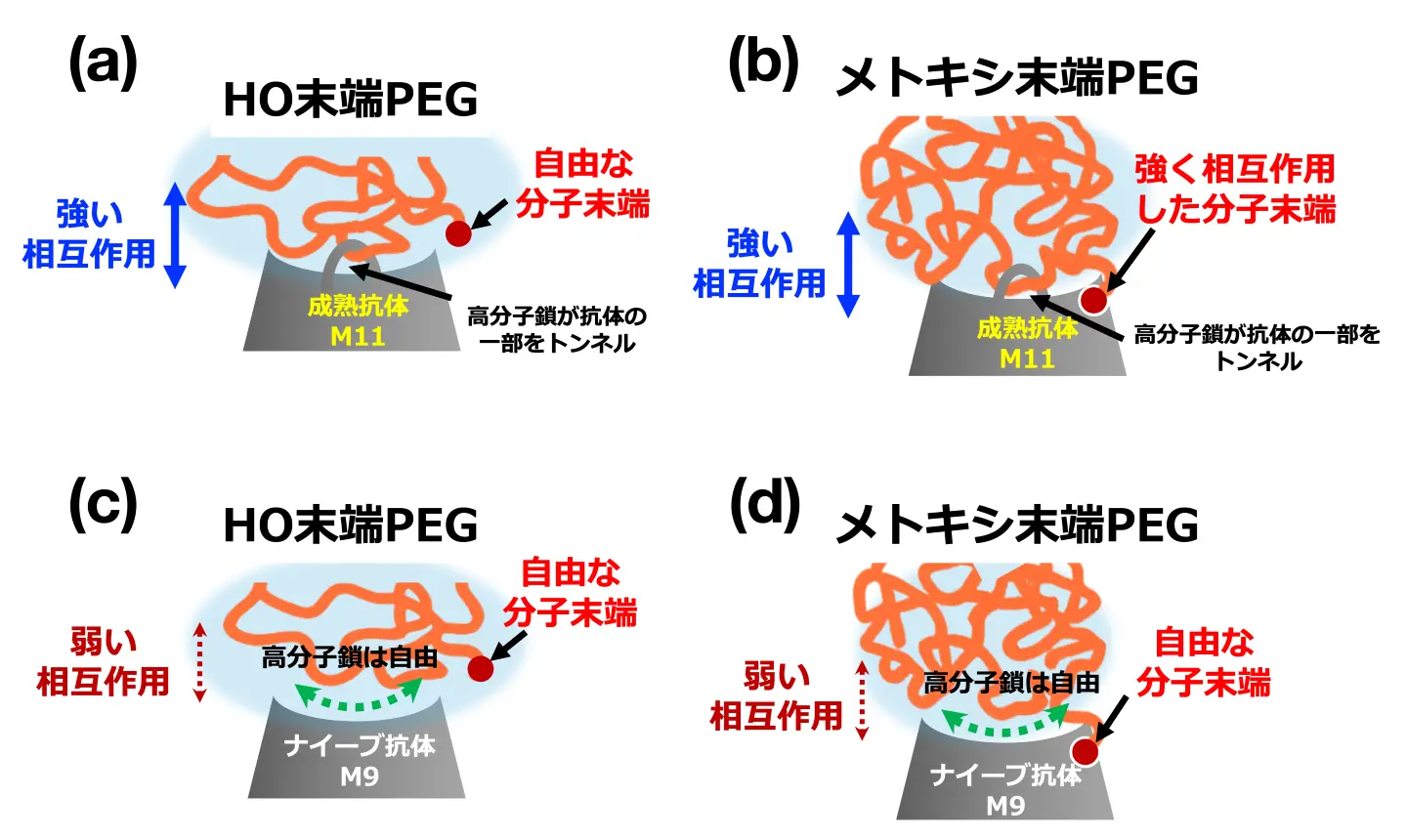
成熟抗体(M11)(図1aおよびb)はそのトンネル状の構造を用いて、PEG鎖を強固に捕捉する一方で、ナイーブ抗体(M9)(図1cおよびd)の結合は弱く、PEG鎖上を滑るような柔軟な結合様式を示しました。 -
末端基による結合力の違い
医薬品で一般的に使用されるメトキシ基末端のPEG(m-PEG)に対しては、両方の抗体がともに強い結合力を示しました(図1bおよびd)。一方、ヒドロキシ基末端のPEG(HO-PEG)に対しては、結合力が低下しました(図1aおよびc)。特に免疫の初期応答で作られるナイーブ抗体は、HO-PEGに対して結合しにくい傾向が顕著でした。 -
水和構造の役割
FTIRとQCM-Dによる解析から、m-PEGは水和が弱く凝縮した構造をとるため抗体がアクセスしやすいのに対し、HO-PEGは周囲に強固で広がりのある水和層(水分子の殻)を形成しており、これが抗体の結合を物理的に阻害していることが示唆されました。
これらの結果から、PEGの「ステルス性」が破られる要因の一つとして、PEG末端の疎水性(メトキシ基)が抗体の足がかりとなっていることが明らかになりました。さらに、親水性の高い末端を用いることで水和バリアを強化し、免疫認識を回避できる可能性が示されました。
社会的インパクト
本研究は、PEG化製剤が免疫系によって排除されてしまう分子メカニズムの一端を解明したものです。現在、多くのDDS製剤では化学的安定性の観点からm-PEGが使用されていますが、本研究成果は、末端をヒドロキシ基(HO-PEG)に変更するか、他の親水性基を導入することで、抗PEG抗体による認識を回避できる可能性を示唆しています。これは、より副作用が少なく、薬効が持続する次世代のナノメディシン開発に貢献する重要な知見です。
今後の展開
今後は、実際の生体環境に近い条件下での検証を進めるとともに、本研究で得られた「水和構造による免疫回避」という指針に基づき、PEGに代わる新しいステルス性高分子や、抗体に認識されにくい新規DDSコーティング材料の設計・開発を目指します。
付記
本研究は、日本学術振興会(JSPS)科学研究費助成事業(JP23H04059、JP22H04530、JP20H05876、JP24K21337)、物質・デバイス領域共同研究拠点、公益財団法人日本台湾交流協会、および防衛装備庁 安全保障技術研究推進制度(JPJ013268)の支援を受けて行われました。
用語説明
- [用語1]
- ポリエチレングリコール(PEG):エチレングリコールが重合した高分子。水によく溶け、生体適合性が高いため、医薬品の安定化や血中滞留性の向上を目的として、薬剤の修飾剤として広く用いられている。
- [用語2]
- 原子間力顕微鏡(AFM):非常に鋭利な探針を用いて試料表面をなぞり、探針と試料の間に働く原子間力を検出することで、ナノメートルオーダーの形状観察や力学物性の測定を行う顕微鏡。本研究では、分子間の結合力を測定する「単一分子力学測定装置」として利用した。
- [用語3]
- 水晶振動子マイクロバランス(QCM-D):水晶振動子の表面に物質が吸着した際の振動数変化とエネルギー散逸変化を測定することで、吸着量だけでなく、吸着膜の粘弾性(硬さや柔らかさ)や水和状態を解析できる装置。
- [用語4]
- フーリエ変換赤外分光法(FT-IR):物質に赤外光を照射し、その吸収スペクトルを測定することで、分子の構造や化学結合の状態を調べる分析手法。本研究では、抗体の結合確認に加え、PEG鎖の周囲に存在する水分子の結合状態(水和構造)の違いを解析するために用いられた。
論文情報
- 掲載誌:
- ACS Applied Bio Materials
- タイトル:
- AFM-based single-molecule force spectroscopy of PEG–anti-PEG antibody interactions
- 著者:
- G. Latag, H. Tahara, A. Katase, S. Maeda, Y. Liu, Y. Kakuta, T. Teramoto, T. Mori, T. Hayashi.
研究者プロフィール
林 智広 Tomohiro Hayashi
東京科学大学 物質理工学院 材料系 准教授
研究分野:表面・界面科学、バイオマテリアル
グレン・ビレナ・ラターク Glenn Villena Latag
東京科学大学 物質理工学院 材料系 大学院生(博士後期課程)
研究分野:表面・界面科学、バイオマテリアル
