ポイント
- 乳児B細胞性急性リンパ芽球性白血病(B-ALL)[用語1]の中で、NUTM1 [用語2] 遺伝子の再構成を有する白血病集団を、独自の遺伝子(ゲノム)[用語3]・エピゲノム[用語4](DNAメチル化[用語5]、クロマチン状態[用語6])特性を持つ独立した集団として定義。
- NUTM1 融合遺伝子(BRD9::NUTM1 など)が、血液細胞を「B細胞へと分化」させつつ、同時に「不死化」させて白血病化させるドライバーであることをマウスモデルで実証。
- NUTM1 再構成白血病は、高リスクな KMT2A [用語7]再構成型白血病とは対照的に、シタラビン(Ara-C)などの化学療法に対して極めて高い感受性を示す特徴を持ち、この治療脆弱性は、白血病幹細胞[用語8]が少なく休眠状態[用語9]を維持できていないという特性に起因することを突き止めた。
- 本研究は、臨床データと基礎研究(生体モデル)を包括的に統合した初めての成果であり、将来的な治療強度の最適化(副作用の低減)や乳児白血病の精密医療(プレシジョン・メディシン)[用語10]の実現に大きく貢献することに期待。
概要
東京科学大学(ScienceTokyo)医歯学総合研究科 発生発達病態学分野の髙木正稔教授、大阪大学 大学院医学系研究科がん病理学教室(同大学院生命機能研究科兼任)の西村耕太郎准教授、井上大地教授、東京大学 大学院医学系研究科 小児医学講座の磯部知弥博士らの共同研究グループは、乳児B細胞性急性リンパ芽球性白血病(B-ALL)において、これまで病態が十分に解明されていなかったNUTM1 再構成を伴うグループの分子病態を包括的に解明し、NUTM1 再構成白血病は、融合相手の遺伝子に依存しない共通の転写・エピゲノム異常を示す独立した疾患群であることを明らかにしました。
乳児に発症する急性リンパ性白血病は、難治性として知られるKMT2A 再構成型が大きな割合を占めます。本研究が対象としたNUTM1 再構成B-ALLは、KMT2A 再構成を欠く症例の中で重要な一群を形成しながらも、その発生機序や臨床的特性は謎に包まれていました。
本研究では、NUTM1 融合遺伝子が、B細胞系列への分化を促進すると同時に、強い白血病幹細胞性を付与するという二重のがん化機構を持つことを発見しました。さらに、代表的な融合遺伝子をマウスで発現させることで、ヒト乳児白血病を忠実に再現する白血病モデルの構築にも成功しました。このマウスを用いた生体試験では、白血病幹細胞が休眠状態に逃げ込まず、常に活発な増殖プログラムに依存しているという本疾患特有の脆弱性に起因することが分かり、本白血病が化学療法に高い感受性を示す分子学的理由を明らかにしました。
本研究成果は、極めて希少で治療選択肢が限られていた乳児白血病において、正確な診断とリスク層別化を可能にするだけでなく、既存薬の有効性を科学的に裏付ける重要な基盤となります。将来的に、個々の症例に応じた治療の最適化を実現し、副作用を最小限に抑えつつ完治を目指す精密医療の進展に大きく貢献することが期待されます。
本研究成果は、米国血液学会の旗艦誌である「Blood 」に、3月26日に公開されました。
井上大地教授のコメント
乳児白血病、特にNUTM1 再構成を伴う症例は、その特異な臨床像と分子背景から近年注目されてきましたが、高頻度に認められるKMT2A 再構成と何がどのように違うのか、初めて包括的に明らかにした研究と言えます。本研究の知見は、単に病気を治すだけでなく、子供たちが治癒した後に健やかな一生を送るための最適な治療をデザインするために不可欠といえます。本研究で見出した知見が、不幸にして白血病を発症した子供たちの健康を守るための医学の発展に寄与することを期待しています。
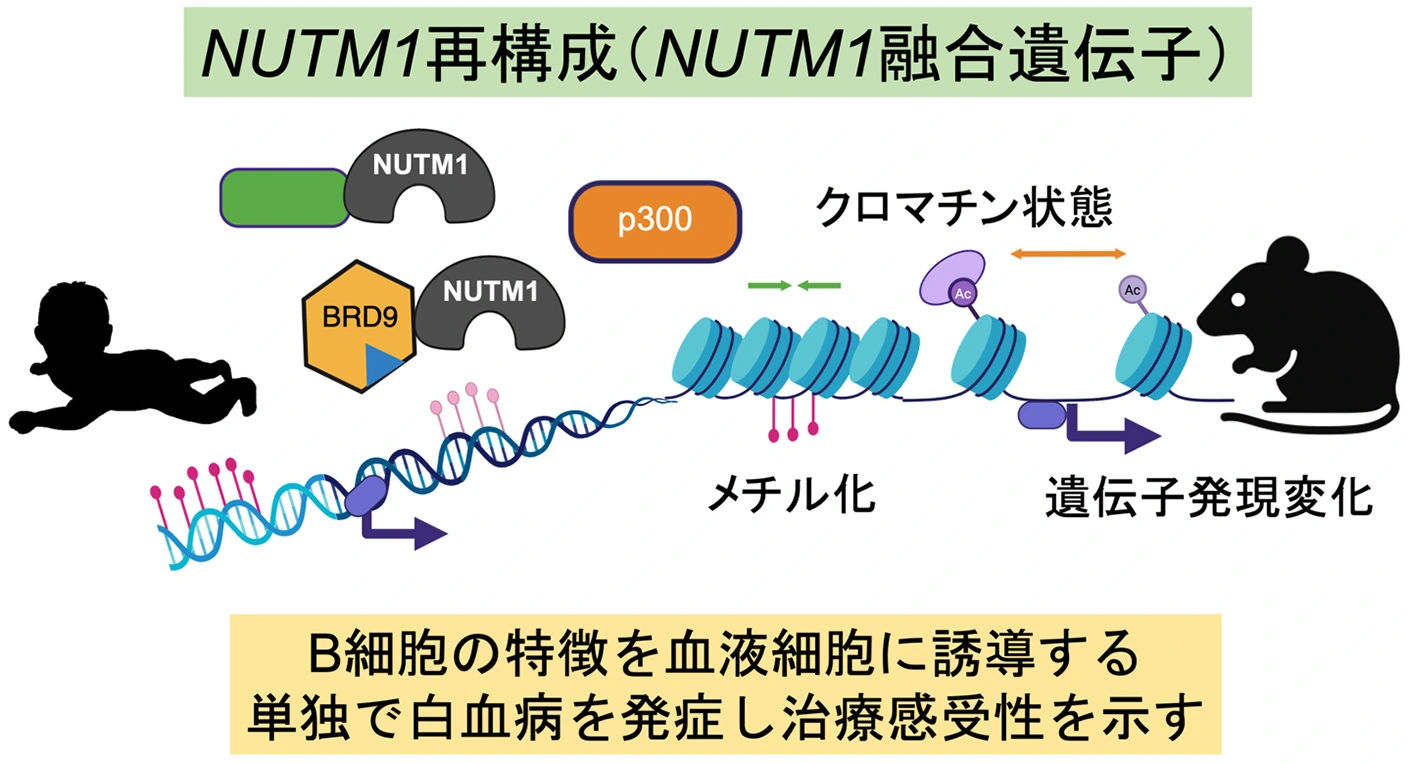
背景
生命維持に不可欠な造血システムは、造血幹細胞を頂点とする精緻な階層構造によって厳密に維持されています。その造血幹細胞に遺伝子、エピゲノムの異常が蓄積することで、細胞分化と細胞増殖の異変により白血病に至ります。その中でも細胞分裂と分化が極めて活発な乳児期に発症する白血病は、成人とは全く異なる遺伝学的背景と臨床経過を辿ることが知られています。特に、生後12か月未満で発症する乳児B細胞性急性リンパ芽球性白血病(B-ALL)の約8割は、難治性のKMT2A 再構成を伴います。
その一方で、近年、KMT2A 再構成を持たない乳児白血病群の中に、いくつかの特徴的なサブタイプが存在することが明らかになってきました。その代表格が「NUTM1 再構成」です。NUTM1 は遺伝子の転座によって様々な融合パートナー遺伝子(転写因子[用語11]、クロマチン制御因子等)と融合することで、多様な組織において強力ながんタンパク質として機能します。
これまでNUTM1 再構成は、きわめて進行が速く侵襲性の高い固形がんである「NUT正中線がん」の主要な原因として注目されてきました。しかし、乳児白血病におけるNUTM1 構成の役割については、一部の臨床報告で「予後が良好である可能性」が示唆されていたものの、なぜこの変異が乳児に特異的に発生するのか、そしてなぜ固形がんとは対照的に治療反応性が高いのかといった根本的なメカニズムは未解明のままでした。
研究成果
1. 臨床データによるNUTM1 再構成白血病の再定義
研究グループは、日本小児がん研究グループ(JCCG)の協力のもと、国内の乳児B-ALL患者検体(MLL96/98, MLL-10コホート)の網羅的解析を行いました。その結果、KMT2A 再構成の無い症例中の4症例(50%)にNUTM1 再構成を同定し、これらがBRD9、AFF1、CHD9 などのパートナーと融合していることを確認しました。さらに、遺伝子発現解析およびDNAメチル化解析を統合し、KMT2A 再構成と比較した結果、NUTM1 再構成白血病は以下の特徴を持つことが明らかとなりました。
- NUTM1 再構成独自の転写の特徴:未分化な血液細胞で見られるCD34 やFLT3 の発現が極めて低く、一方でNUTM1 自身やB細胞分化に関わる遺伝子群が高発現していました。KMT2A 再構成型が未分化な特徴を持つのに対し、NUTM1 再構成は、より「B細胞系譜へ分化した特徴」を示しました。
- NUTM1 再構成独自のクロマチン(DNAメチル化)の特徴:NUTM1 再構成における低メチル化領域にはEBF1 やMEF2C といったB細胞分化の重要因子の結合部位が濃縮しており、これらが転写の特徴でも見られた「B細胞としての特徴」を支持していると考えられます。
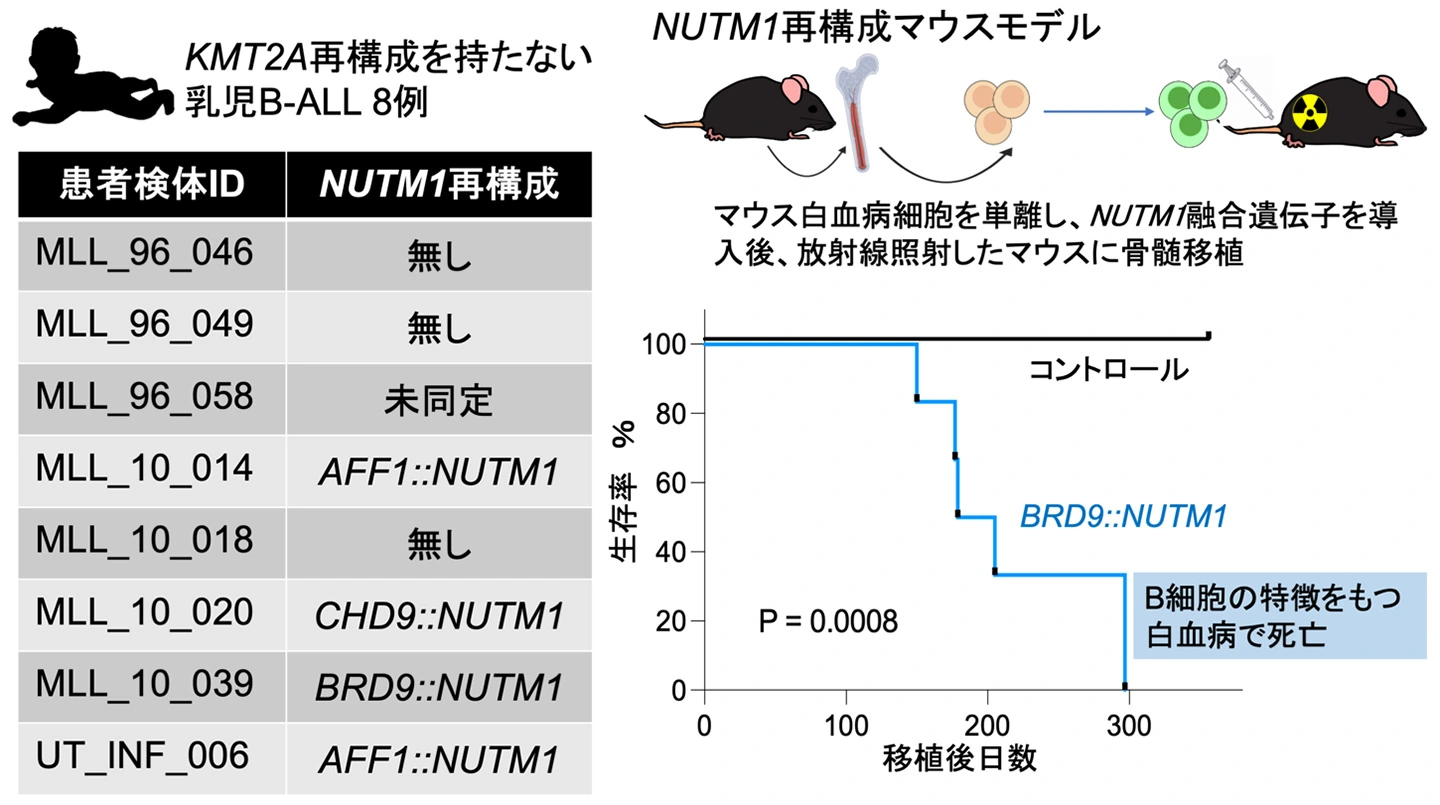
2. 生体モデルによるNUTM1 再構成の機能検証
次に、NUTM1 融合遺伝子のB細胞分化、白血病発症における役割を検証するため、マウスの造血幹・前駆細胞を用いた生体モデルを構築しました。
- NUTM1 融合遺伝子によるB細胞分化:リンパ球細胞に分化可能な iLS細胞[用語12]にNUTM1 再構成遺伝子を導入したところB細胞分化が促進されました。
- 白血病の発症、ヒト表現型の再現:マウスの骨髄の幼若な幹細胞に融合遺伝子を導入して移植したところ、患者検体の解析でも同定されたBRD9::NUTM1 の導入マウスがB細胞の細胞表面抗原(B220+, CD43+, CD19-, IgM-)を示し、ヒトの病態に極めて類似した表現型を示しました。これは、BRD9-NUTM1 単独で発がんを誘導できる強力なドライバーであることを示しています。
- 自己複製能、不死化の獲得:連続移植実験により、BRD9::NUTM1 白血病細胞は自己複製能を有する白血病幹細胞を有し、無限の増殖能を持つことが示されました。
3. クロマチン構造の変化とメカニズムの解明
なぜBRD9-NUTM1 は、細胞をB細胞系譜に誘導し、がん化させるのか、以下の2点に着眼しました。
- クロマチン制御の重要性:BRD9は本来、ncBAF複合体[用語13]の構成因子としてクロマチン制御を担っています。マウス実験で、BRD9::NUTM1 による白血病化はこのncBAF複合体と、NUTM1 と転写の活性化に関与するヒストンアセチル化酵素p300との相互作用が重要であることが明らかとなりました。
- B細胞分化と白血病化の共存:メチル化解析、ATAC-seq[用語14]、ChIP-seq[用語15]解析によりクロマチン状態を解析したところ、B細胞に重要なシグナル、HOXA9およびMEIS1のような幹細胞性プログラムが同時に活性化しており、これが「B細胞の特徴を有した白血病」という特異な性質を生み出している根源であることが判明しました。
4. 治療的脆弱性の発見と臨床への意義
本研究は、さらにNUTM1 再構成白血病と治療感受性の理由を解明に努めました。360種類の薬剤を検証した結果、BRD9::NUTM1 細胞は、核酸合成阻害剤(シタラビン、アザシチジン、RNAポリメラーゼII阻害剤など)に対して顕著に高い感受性を示しました。マウスモデルを用いた生体試験では、KMT2A 再構成型白血病がシタラビン投与にほとんど反応せず早期に白血病により死亡するのに対し、BRD9::NUTM1 白血病マウスは劇的な生存期間の延長を示したのです。この脆弱性の理由は、白血病幹細胞の「休眠状態」の欠如にあると考えられます。KMT2A 再構成などの高リスク白血病では、白血病幹細胞が一時的に細胞周期[用語16]を抑制し休眠状態に入ることで薬から逃れます。BRD9-NUTM1 白血病は、元々の白血病幹細胞が少ない上、細胞周期を抑制する因子(p21, p57, p16など)が著しく低下しており、休むことができません。これが化学療法に対する「逃げ場」を失わせていると考えています。
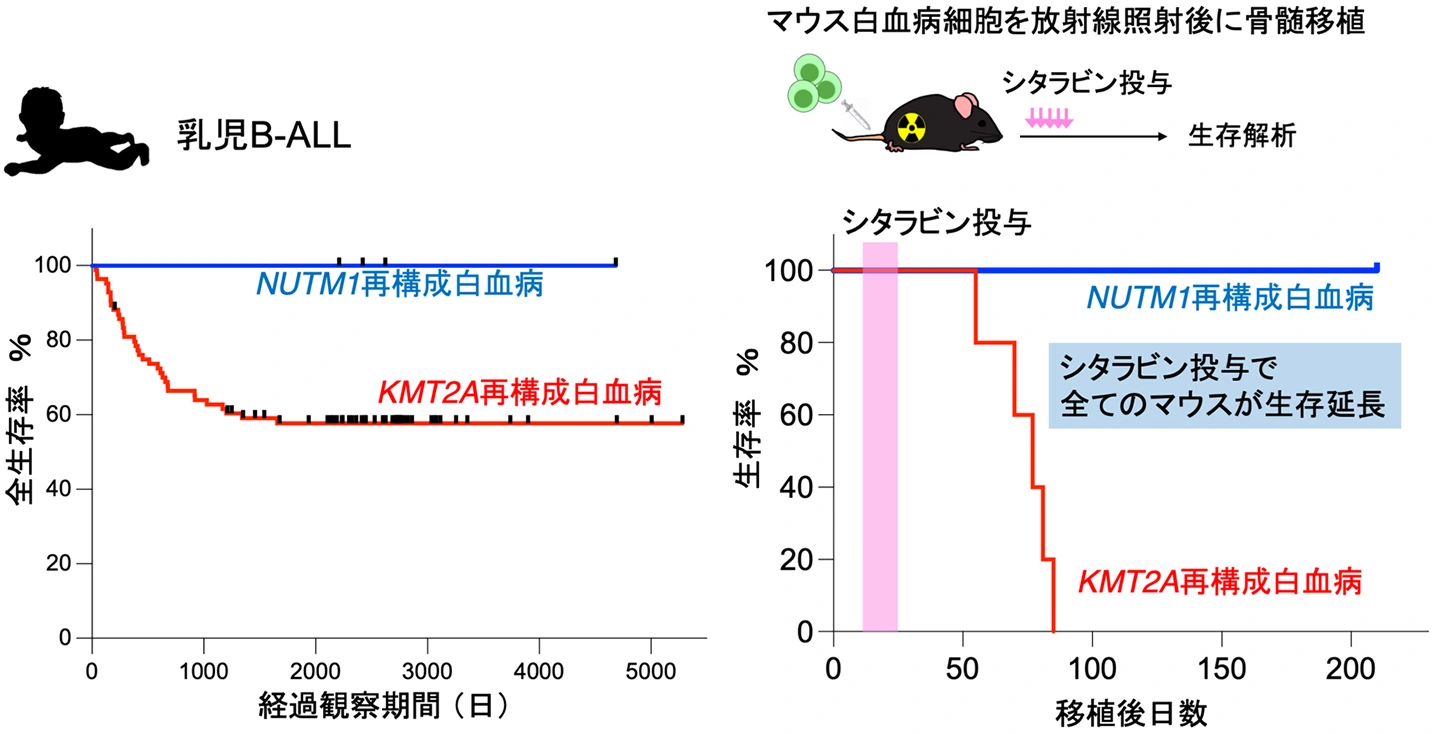
社会的インパクト
本研究成果は、乳児白血病の医療現場に、以下のような大きな進展をもたらすことが期待されます。
1. 精密なリスク層別化と診断の標準化
乳児B-ALLにおいて、NUTM1 再構成を正確に診断することで、その症例が「化学療法によく反応する良好なグループ」であることを事前に予測できます。これにより、患者や家族に対する予後の説明がより正確になり、不要な治療(造血幹細胞移植など)を回避できる可能性があります。
2. 治療の最適化による晩期合併症の低減
乳児期に行われる強力な化学療法は、寛解後の心機能異常、発達障害、不妊、二次がんなどの重篤な晩期合併症を引き起こすリスクがあります。本研究で示されたシタラビン等薬剤への高い感受性に基づき、将来的には治療強度を適切に弱めつつ、根治を目指すプレシジョン・メディシンの開発に繋がります。
3. 新規治療標的の同定
本研究で注目したBRD9やp300といったエピジェネティック因子の制御が、NUTM1 再構成白血病の維持に必須であることが示されたため、これらの阻害剤を用いた新しい低毒性療法の開発が期待されます。これは、白血病だけでなく、同じくNUTM1 融合を伴う固形がん(NUT正中線がん)への応用も視野に入れた画期的な展開の可能性を有しています。
付記
本研究は、日本学術振興会(JP20H00537, JP20H03717, JP22H04922(AdAMS), 16H06279(PAGS), JP23K07824, JP24H00866, JP23H0043, JP24K21298)、科学技術振興機構(JPMJCR23B7)、日本医療研究開発機構(AMED)(JP21ck0106697, JP22ck0106697, JP23ck0106697, JP23ama221126, JP15cm0106139, JP20cm0106572, 23ama221514, JP24ama221135)、 日本血液学会、米国血液学会、内藤記念科学振興財団、三菱財団、住友財団、千里ライフサイエンス振興財団、武田科学振興財団、化学及血清療法研究所、白血病研究基金を育てる会、高松宮妃癌研究基金、持田記念医学薬学振興財団、 MSD生命科学財団、アステラス病態代謝研究会、小児医学研究振興財団、船井情報科学振興財団、本庄国際奨学財団、米国Leukemia & Lymphoma Society、米国NIH(R01CA242020, R01CA25113, R01HL128239, P50CA254838, P30CA046934, R01CA269269)、米国The Edward P. Evans MDS Foundation、米国The Bristol Myers Squibb Foundation、米国The Morgan Adams Foundation の支援によって行われました。
データ解析において東京大学医科学研究所ヒトゲノム解析センターのスーパーコンピュータ「SHIROKANE」を利用しました。
用語解説
- [用語1]
- 乳児B細胞性急性リンパ芽球性白血病(B-ALL):生後1歳未満に発症するB細胞系の血液腫瘍。進行が非常に速く、成人の白血病とは異なる特有の遺伝子異常(KMT2A再構成)を伴うことが知られています。
- [用語2]
- NUTM1:NUT midline carcinoma family member 1。クロマチン調節、特にアセチル化に関与します。この遺伝子が他の遺伝子と融合する異常(遺伝子転座、再構成)を起こすと、悪性度の高いNUT正中線がんを代表とする「NUTがん」を引き起こすことが知られています。
- [用語3]
- 遺伝子(ゲノム):生命体の細胞内に存在する「タンパク質の作り方」や「生命体の特徴(表現型)」を決定する設計図のことを遺伝子といい、その総称をゲノムと言います。ヒトなどの真核生物のゲノムは核内に存在するDNA塩基(デオキシリボ核酸、アデニンA、グアニンG、シトシンC、チミンT)の並び(塩基配列)として構築されており、RNAへ写し取られ(転写)、タンパク質に変換(翻訳)されることで機能を発現します。次世代(親から子)へと引き継がれ(遺伝)、生命活動を支えています。
- [用語4]
- エピゲノム:DNA塩基配列を変えずに遺伝子が機能発現する活性を制御する仕組み(エピジェネティクス)によりゲノムに付加された遺伝情報のこと。
- [用語5]
- DNAメチル化:DNAの塩基配列(主にシトシン)にメチル基(−CH3)が付加される修飾で、機能発現を抑制する役割を持つエピゲノムの一種です。遺伝子の「オン/オフ」スイッチとして機能しています。
- [用語6]
- クロマチン状態:細胞の核内でDNAがヒストンと呼ばれるタンパク質と結合した複合体(クロマチン)の、構造的な密度や折り畳み、構成するタンパク質の修飾のこと。クロマチン状態は遺伝子発現のスイッチを制御するエピゲノム情報として知られています。
- [用語7]
- KMT2A:ヒストンのメチル化を介してクロマチン状態、遺伝子発現を制御する酵素をコードする遺伝子です。この遺伝子の染色体転座や融合は、特に乳児白血病の原因因子として知られています。
- [用語8]
- 白血病幹細胞:白血病細胞を生み出す源となる細胞。自己複製能力を持ち、抗がん剤への抵抗性が高いため、再発の根本原因と考えられています。
- [用語9]
- 休眠状態:細胞が分裂を停止し静止している状態。抗がん剤は細胞の分裂メカニズムを標的とする薬剤が多く、休眠状態の細胞は治療を逃れやすいことが知られています。
- [用語10]
- 精密医療(プレシジョン・メディシン):患者一人ひとりの遺伝子変異や病態を詳細に分析し、その特徴に最も適した薬剤や治療法を選択する医療のこと。
- [用語11]
- 転写因子:DNAの特定の配列に結合し、遺伝子の転写(RNA書き出し)のON/OFF(転写の開始や抑制)を制御するタンパク質のこと。
- [用語12]
- iLS細胞:iLS細胞(induced Leukocyte Stem cell:人工白血球幹細胞)は、造血幹・前駆細胞から作られ、多様な白血球(リンパ球、マクロファージなど)へ分化する能力を持ち、試験管内で無限に増幅・維持可能な多能性前駆細胞です。
- [用語13]
- ncBAF複合体:クロマチン状態を制御するタンパク質複合体(SWI/SNF複合体)の一つ。SWI/SNF複合体ファミリー全体は、29種類のタンパク質の組み合わせで構成され、現在は3つのサブファミリー、canonical BRG1/BRM-associated factor(cBAF)、polybromo-associated BAF(PBAF)、最近発見されたnon-canonical BAF(ncBAF)が同定されています。
- [用語14]
- ATAC-seq:クロマチンの構造が緩んでいる(アクセスしやすい)場所を特定し、どの遺伝子領域が活性化しうるかを調べる解析手法のこと。
- [用語15]
- ChIP-seq:特定のタンパク質(転写因子、クロマチン制御因子など)がDNAのどこに結合しているかを網羅的に調べ、遺伝子制御の仕組みを可視化する手法のこと。
- [用語16]
- 細胞周期:一つの細胞が成長し、DNAを複製して二つの細胞に分裂するまでの一連の過程。DNAを複製するS期、細胞が分裂するM期、およびそれらの間にある準備期間(G1期、G2期)に分かれます(G1, S, G2期を総称して間期と呼びます)。
論文情報
本研究成果は、2026年3月26日に米国科学誌「Blood」(オンライン)に掲載されました。
- 掲載誌:
- Blood
- タイトル:
- Comprehensive Molecular and Functional Analysis of NUTM1-Rearranged Leukemia
- 著者:
- Koutarou Nishimura*, Tomoya Isobe*, Weijia Zang, Muran Xiao, Masaki Nomura, Yui Koike, Tsukasa Shigehiro, Akira Nishimura, Aiko Sato-Otsubo, Hiromi Yamazaki, Hiromi Ito, Wataru Saika, Yifan Zhang, Yumi Aoyama, Chihiro Hasegawa, Takaya Yamasaki, Yasuo Kubota, Kentaro Ohki, Nobutaka Kiyokawa, Genta Nagae, Kenichi Yoshida, Yasuhito Nannya, Hiroo Ueno, Shiro Fukuda, Kenji Tatsuno, Shuichi Tsutsumi, Yusuke Shiozawa, Yuichi Shiraishi, Kenichi Chiba, Hiroko Tanaka, Mariko Eguchi, Yuki Arakawa, Katsuyoshi Koh, Daisuke Tomizawa, Takako Miyamura, Eiichi Ishii, Shuki Mizutani, Satoru Miyano, Hiroyuki Aburatani, Seishi Ogawa, Akifumi Takaori-Kondo, Akihiko Yokoyama, Omar Abdel-Wahab, Junko Takita, Tomokatsu Ikawa, Masatoshi Takagi†, Daichi Inoue†.(*同等の寄与、†責任著者)