血液中の微粒子が「腎臓病」と「心血管病」の将来のリスクを予言する
細胞外小胞内マイクロRNAの解析により慢性腎臓病と合併症リスクを高精度に予測する新技術を開発
ポイント
- 血液中の小型細胞外小胞(EV)内のマイクロRNAを解析し、慢性腎臓病(CKD)および心血管合併症の長期的なリスクを高精度で予測する新技術を開発した。
- 開発した予測モデルは、腎機能、尿蛋白など従来の指標を上回り、CKDの原因疾患の種類や心血管疾患の有無にかかわらず有効であった。
- EV内マイクロRNAの不足やEVの受容細胞における分子シグナル変化の解明につながり、CKDと心血管疾患の病態解明・個別化医療への貢献が期待される。
概要
東京科学大学(Science Tokyo)大学院医歯学総合研究科 腎臓内科学分野の萬代新太郎准教授(テニュアトラック)、稲葉俊介大学院生(博士課程3年)、内田信一教授らの研究チームは、総合研究院M&Dデータ科学センターの長谷川嵩矩准教授との共同研究により、慢性腎臓病(CKD)および心血管合併症の長期的な発症・進展リスクを予測する新たな技術を開発しました。
研究チームは、CKDの患者集団を対象に、血液中の小型細胞外小胞(EV)[用語1]に内包されるマイクロRNA[用語2]の量を網羅的に調べました。さらに、機械学習アルゴリズムを用いて、CKDおよび心血管合併症に関与するマイクロRNAを抽出しました。
その結果、特定のマイクロRNA群の量が不足していることが、CKDおよび心血管合併症のリスク上昇と関連していることが明らかになりました。そのうちの3種類のマイクロRNAを組み合わせた予測式は、従来になく高い予測精度を示しました。
EV内マイクロRNAが減少する仕組みや、EVを受容する細胞における分子シグナル変容の解明に向けた基礎となる本研究は、近年注目されている心血管・腎・代謝症候群(CKM シンドローム)[用語3]の概念にも通じるものであり、腎臓病を軸とした臓器連関による全身疾患のメカニズム解明に貢献する重要な知見です。
今後は、本研究で得られた成果をもとに、診療現場で日常的に活用できるリスクスコアとしての実用化を進め、CKD患者の予後改善に貢献することを目指します。
本成果は、12月10日付(現地時間)でアメリカ心臓協会の国際学術誌「JAHA: Journal of the American Heart Association」に掲載されました。
背景
わたしたちの腎臓は、進化の過程で老廃物の排泄にとどまらず、ミネラルや血圧の調整、赤血球をつくる造血ホルモンの産生、さらには骨の強化など、生命と健康を維持するための幅広い役割を担うようになりました。
長寿社会となった現代では、腎臓は老化や高血圧症、糖尿病など、さまざまな要因によって機能が低下します。症状を自覚しにくい慢性腎臓病(CKD)は、静かに発症・進行し、本邦では2,000万人以上(高齢者の約3人に1人)、世界では8億5千万人以上が罹患しているとされています。
本研究グループはこれまで、腎臓病を起点として全身に波及する複雑な病態(multi-morbidity/多併存症)[参考文献1]や、“腎性老化(腎臓病によって老化が加速する現象)[参考文献2]”の解明に取り組んできました。「腎臓が寿命を決める」ともいわれるその所以を明らかにするため、生物学的なメカニズムの解明と、透析に代わる治療薬の創薬を目指しています。
近年では、CKDは腎臓だけでなく心血管や代謝にも悪影響を及ぼすことから、これらをまとめて心血管・腎・代謝症候群(CKMシンドローム)と呼ぶ概念も注目されています。しかし、病気の進行や心血管合併症の長期的リスクを正確に予測する指標や、分子メカニズムはいまだ十分に確立されていません。
そこで本研究では、血液中を循環する小型細胞外小胞(EV)に含まれるマイクロRNAに注目しました。EVは血液1 ccあたり10億個以上存在し、細胞間でメッセージ物質を運搬します。これらがCKDの進行や臓器間の有害な連関に関与する可能性について検討しました。
研究成果
本研究では、慢性腎臓病(CKD)患者36名からなる集団(導出コホート)において、循環EVに含まれるマイクロRNAをトランスクリプトーム解析[用語4]により網羅的に評価しました。その結果、特定のマイクロRNA群の量が不足していることが、CKDおよび心血管合併症のリスク上昇と関連していることが明らかになりました。
Lasso-Cox解析[用語5]により予測モデルを構築したところ、3種類のマイクロRNA(hsa let 7d 5p, hsa miR 24 3p, hsa miR 126 3p)を組み合わせた予測式「M3予測式」が、(1)推定糸球体濾過量(eGFR)の30%低下、(2)透析開始、のいずれかからなる「腎臓アウトカム」を高い精度で予測できることを示しました。
さらに大規模な独立検証集団(検証コホート)を用いてモデルを再評価し、前述の3種類のマイクロRNAに血中シスタチンCおよび尿蛋白量を加えた改良モデル「M3V2予測式」を確立しました(図1)。
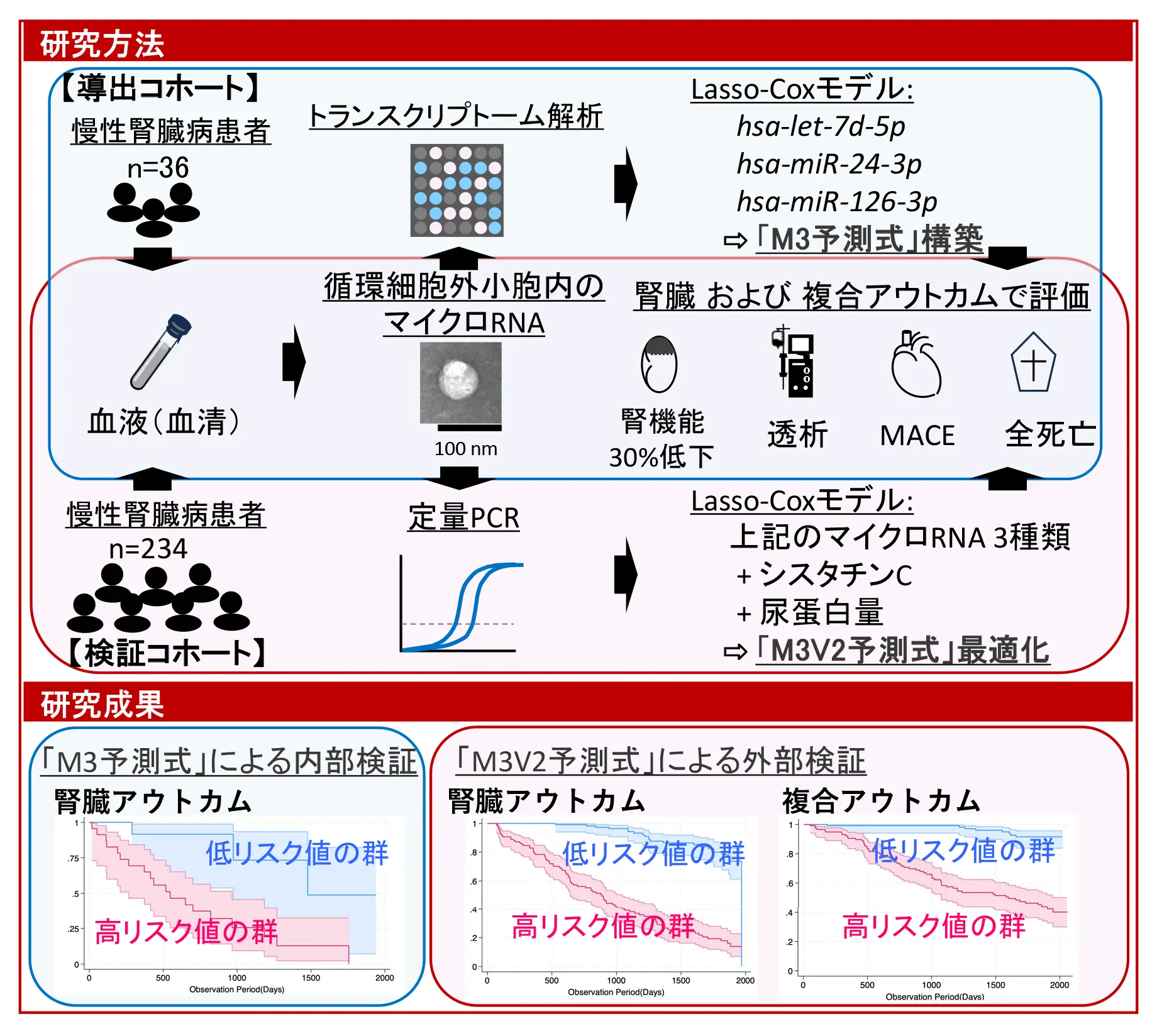
M3V2スコアが高値の群では、前述の「腎臓アウトカム」に加え、(1)全死亡、(2)主要心・脳血管イベントによる入院、(3)透析開始、のいずれかからなる「複合アウトカム」の発生リスクが有意に高く、これらを高精度で予測できることが示されました。
本モデルは、腎機能や尿蛋白量といった従来の単変数指標を上回る予測能を示し、さらに層別解析の結果、CKDの原因疾患の種類や心血管疾患の有無によらず普遍的に有効であることが確認されました。
コンピューターベースの解析結果では、健康な状態のEVに豊富に含まれるマイクロRNAが、標的細胞の老化シグナルなどを抑制する“セーフガード”として機能していることが示唆されました。一方、CKDではこのセーフガードが失われている、すなわちEVの「機能低下」が生じている可能性が示されました。これにより、腎疾患のみならず腎外臓器の障害メカニズムにも関与しうることが示唆されました。
実際に、前述の3種類のマイクロRNAそれぞれを詳細に解析したところ、量が不足している患者では、心血管疾患の既往や高血圧症の合併、利尿薬・降圧薬・糖尿病薬の使用、貧血治療の必要性など、腎臓のみならず心血管系・代謝系といった全身にかかわる合併症が多いことが明らかになりました(図2)。
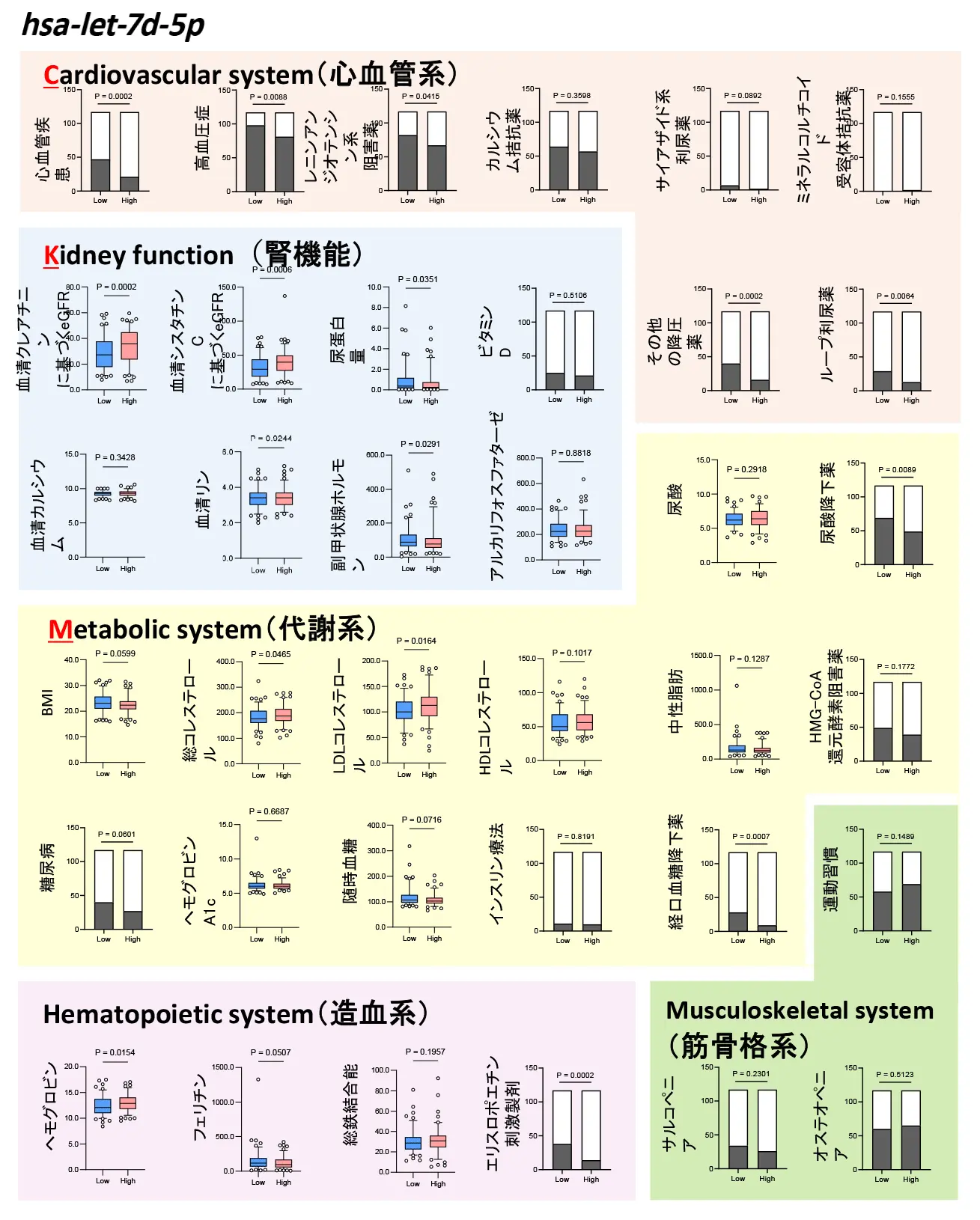
つまり、マイクロRNAのプロファイルはEVの機能を反映しており、心腎代謝症候群の病態に深く関与している可能性があります。これらのマイクロRNAは、本症候群の新たな分子マーカーとなるだけでなく、病態解明に向けた新たな道を拓く可能性を示しています。
社会的インパクト
医療の発展により、今後さらに長寿社会が進展するなかで、慢性腎臓病(CKD)の発症および罹患者数は増加していくと予想されます。そのため、CKDとその合併症を的確に診断し、適切に治療することの重要性はますます高まると考えられます。
本研究では、血液検査で得られるEV中のマイクロRNAを用いるという、患者への負担が少ない方法により、将来の腎機能悪化や心血管合併症のリスクをより正確に予測できる新しい技術を開発しました。
この技術により、リスクの高い方々を早期に抽出し、積極的な治療介入を行うことで、将来の透析開始リスクや重大な心血管イベントを減らすことが可能となり、個別化医療の実施に大きく貢献することが期待されます。
今後の展開
本研究は単一施設(当大学病院)で実施されたものであり、対象は当院を受診した日本人CKD患者に限られています。今後は、協力施設を拡大し、さまざまな人種・民族を含むより大規模な集団で検証を進め、予測モデルのさらなる汎化可能性を評価する予定です。さらに予測モデルを用いた患者層別化に基づく介入試験を実施し、リスクスコアに基づく治療介入が臨床転帰を改善するかどうかを検証することによって、最終的には、診療現場で日常的に活用できるリスクスコアとして実用化することを目指します。このため、検査の簡便化・標準化および検査費用の妥当性についても検討を進めていきます。
また、CKD患者において循環EV内マイクロRNAの不足が生じる機序や、循環EVを介した受容細胞での分子シグナル変容を詳細に解析し、新たな視点からCKDおよび併存する心血管疾患の病態解明に取り組みます。これにより、マイクロRNAの補充や循環EV機能の修復などを含む新規治療戦略の基礎を築くことを目指します。
本研究は、血液中の微小粒子に含まれる分子情報が、腎臓病および心血管・代謝合併症の将来リスクを予測しうることを示した重要な一歩です。今後の研究と臨床応用の発展により、CKD患者の予後改善に貢献することを目指します。
付記
本研究は、科学技術振興機構(JST)創発的研究支援事業FOREST (JPMJFR225O)、JST 戦略的創造研究推進事業 ACT-X「生命と化学」(JPMJAX191)、国立研究開発法人日本医療研究開発機構(AMED)腎疾患実用化研究事業(不良細胞外小胞を標的とした慢性腎臓病と腎性老化現象の病態解明; JP24ek0310025)、文部科学省科学研究費補助金(20K16514、22H02966、23K24346、24K22093)、公益財団法人中冨記念財団、東京医科歯科大学 次世代研究者育成ユニット、日本透析医会、公益財団法人薬力学研究会、公益財団法人武田科学振興財団、JST次世代研究者挑戦的研究プログラム(SPRING)(JPMJSP2180)による支援を受けて実施されました。
参考文献
- [1]
- Mandai S, et al. Burden of kidney disease on the discrepancy between reasons for hospital admission and death: An observational cohort study. PLoS One. 2021; 16(11): e0258846.
プレスリリース:全国規模の入院データ解析により慢性腎臓病(CKD)の複雑病態を可視化|旧・東京医科歯科大学 - [2]
- Koide T, et al. Circulating Extracellular Vesicle-Propagated microRNA Signature as a Vascular Calcification Factor in Chronic Kidney Disease. Circ Res. 2023; 132(4): 415-431.
プレスリリース:慢性腎臓病において血管石灰化を引き起こす悪玉メッセージ物質を発見|旧・東京医科歯科大学
用語説明
- [用語1]
- 小型細胞外小胞(EV、small extracellular vesicles):全ての細胞種から放出される、脂質二重層からなる直径200ナノメートル以下の小胞で、タンパク質・脂質・核酸などを内包する。血液や組織間を移動して他の細胞に分子群、いわばメッセージ物質を届けることでシグナル伝達や免疫応答の調節に関与し、疾患のマーカーや薬物送達の手段として注目されている。
- [用語2]
- マイクロRNA:長さ約20〜24塩基の短い非翻訳RNAで、標的となるメッセンジャーRNAに結合してその翻訳を抑制、分解を促進することで遺伝子発現を負に制御する。ヒトでは2,500種類程度(本研究時点)が同定されており、多岐にわたる遺伝子ネットワークに関与し、細胞分化・増殖・アポトーシスや疾患の発症・進展に重要な役割を果たすため、バイオマーカーや治療標的として注目されている。
- [用語3]
- 心血管・腎・代謝症候群(CKMシンドローム):心血管疾患、慢性腎臓病、肥満に代表される代謝疾患の相互作用による疾患概念。近年アメリカ心臓協会によって提唱され、特に高い心血管疾患率や死亡率と関わることから、注目されている。
- [用語4]
- トランスクリプトーム解析:細胞や組織内で発現しているすべての転写産物の種類と量を網羅的に測定して、遺伝子発現プロファイルを把握する手法。近年、疾患メカニズムの解明やバイオマーカー探索など多方面で活用されている。
- [用語5]
- Lasso-Cox解析:生存時間やイベント発生までの時間を扱うCox比例ハザードモデルにL1正則化(Lasso)を組み合わせ、予測に有用な変数を自動で選択しつつ過学習を抑える機械学習の一手法。多数の候補変数がある状況で重要な因子を絞り込み、リスク予測モデルを構築する際に有効である。
論文情報
- 掲載誌:
- JAHA: Journal of the American Heart Association
- タイトル:
- Circulating Extracellular Vesicle MicroRNAs as Predictive Biomarkers for Kidney and Cardiovascular Events
- 著者:
- Shunsuke Inaba, Takanori Hasegawa, Yuta Nakano, Shotaro Naito, Rena Suzukawa, Takaaki Koide, Hisateru Sekiya, Hisazumi Matsuki, Tamami Fujiki, Hiroaki Kikuchi, Yohei Arai, Yutaro Mori, Fumiaki Ando, Takayasu Mori, Koichiro Susa, Soichiro Iimori, Eisei Sohara, Shinichi Uchida, Shintaro Mandai
研究者プロフィール
萬代 新太郎 Shintaro Mandai
東京科学大学 大学院医歯学総合研究科 腎臓内科学 准教授(テニュアトラック)
研究分野:腎臓、水・電解質輸送、サルコペニア、細胞外小胞
稲葉 俊介 Shunsuke Inaba
東京科学大学 大学院医歯学総合研究科 腎臓内科学 大学院生
研究分野:腎臓、細胞外小胞、臓器間相互作用
長谷川 嵩矩 Takanori Hasegawa
東京科学大学 総合研究院M&Dデータ科学センター 准教授
研究分野:生命情報学、統計科学
内田 信一 Shinichi Uchida
東京科学大学 大学院医歯学総合研究科 腎臓内科学分野 教授
研究分野:腎臓、水・電解質輸送