ポイント
- 脳腫瘍を正確に見分けるタグ(荷札)分子と、ワインに含まれる“タンニン酸”を用いて、アデノ随伴ウイルスベクター(AAV)を搭載した脳腫瘍標的型ナノマシンを創成。
- 標的型ナノマシンによって、AAVを脳腫瘍へ選択的に届けることに成功。投与量の大幅削減による、高い有効性と安全性を動物モデルで実証。
- 本研究成果は、AAVを用いた効率的かつ安全ながん遺伝子治療のための新しいアプローチとして臨床応用が期待される。
概要
東京科学大学(Science Tokyo)総合研究院 化学生命科学研究所の松平望(当時 大学院博士課程学生)、本田雄士助教(川崎市産業振興財団ナノ医療イノベーションセンター<iCONM>主任研究員兼任)、西山伸宏教授(同主幹研究員兼任)、iCONM 喜納宏昭博士(同主幹研究員)、東京大学医科学研究所遺伝子・細胞治療センター 分子遺伝医学分野の喜納(早下)裕美特任助教、岡田尚巳教授らのグループが共同で、脳腫瘍にピンポイントでアデノ随伴ウイルスベクター(AAV)[用語1]を送達する標的型ナノマシン[用語2]を開発しました。この標的型ナノマシンは、がん細胞特異的に結合するタグ(荷札)分子、ワインなどの渋み成分であるタンニン酸[用語3]、そして精密合成高分子から構成されています。これにより、生体内での中和抗体や免疫反応からAAVを保護しつつがん細胞まで選択的に送達し、AAV 自体の高い活性を維持したまま、がん細胞内でのみAAVを放出することが可能となります。
AAVは、遺伝子治療用ベクターとして臨床応用され近年期待が高まっていますが、がん治療においては、患部への不十分な集積と高容量投与による深刻な肝毒性が課題となります。今回、新たに開発した標的型ナノマシンを用いて、AAVを脳腫瘍へ選択的に届けることに脳腫瘍モデルマウスで成功し、従来の3分の1の投与量で高い安全性と有効性を実証することができました。
本研究成果は、これまで治療の選択肢が限られていた悪性の脳腫瘍に対して、AAVベクターを利用した遺伝子治療という新たな治療アプローチを提案し、今後の臨床応用が期待されます。
本研究成果は2025年11月29日(米国東部時間)「Journal of Controlled Release」誌にオンライン掲載されました。
背景
遺伝子治療とは、遺伝子または遺伝子を導入した細胞を人の体内に投与し、体内で不足するタンパク質を補足したり、その働きを助けたりすることにより疾患の治療を行う新たな治療法です。その中で、ウイルスベクターは、ウイルスが細胞に感染する機構を利用して遺伝子を体内に運ぶ運搬体の1つとして利用されています。中でもアデノ随伴ウイルスベクター(AAVベクター)は、様々な細胞種に遺伝子導入が可能であり、長期的に遺伝子発現が継続することから、脊髄性筋萎縮症、デュシェンヌ型筋ジストロフィー、血友病など様々な難治性疾患に対して臨床応用されています。しかしながら、がん治療においては、標的であるがんへの集積性が低く、肝臓や腎臓など健康な臓器への望まない集積により深刻な副作用が引き起こされる可能性があります。また、成人の大半がAAVに対する中和抗体を自然に持っており、投与可能な患者が制限されていることも課題としてあげられています。
このような課題に対して、ウイルスベクターのカプシド[用語4]を遺伝子編集して標的性を持たせたり、ウイルスベクターの表面をポリエチレングリコール(PEG)で修飾して中和抗体を回避したりする試みがなされています。しかしながらこれらの方法は、ウイルスベクター自体の細胞内取り込み能力を阻害してしまい遺伝子導入効率が低下してしまいます。従って、AAVの高い遺伝子導入効率を維持したまま、AAVをがん細胞選択的に送達し、かつ中和抗体を回避できるAAV送達システムが求められています。
研究成果
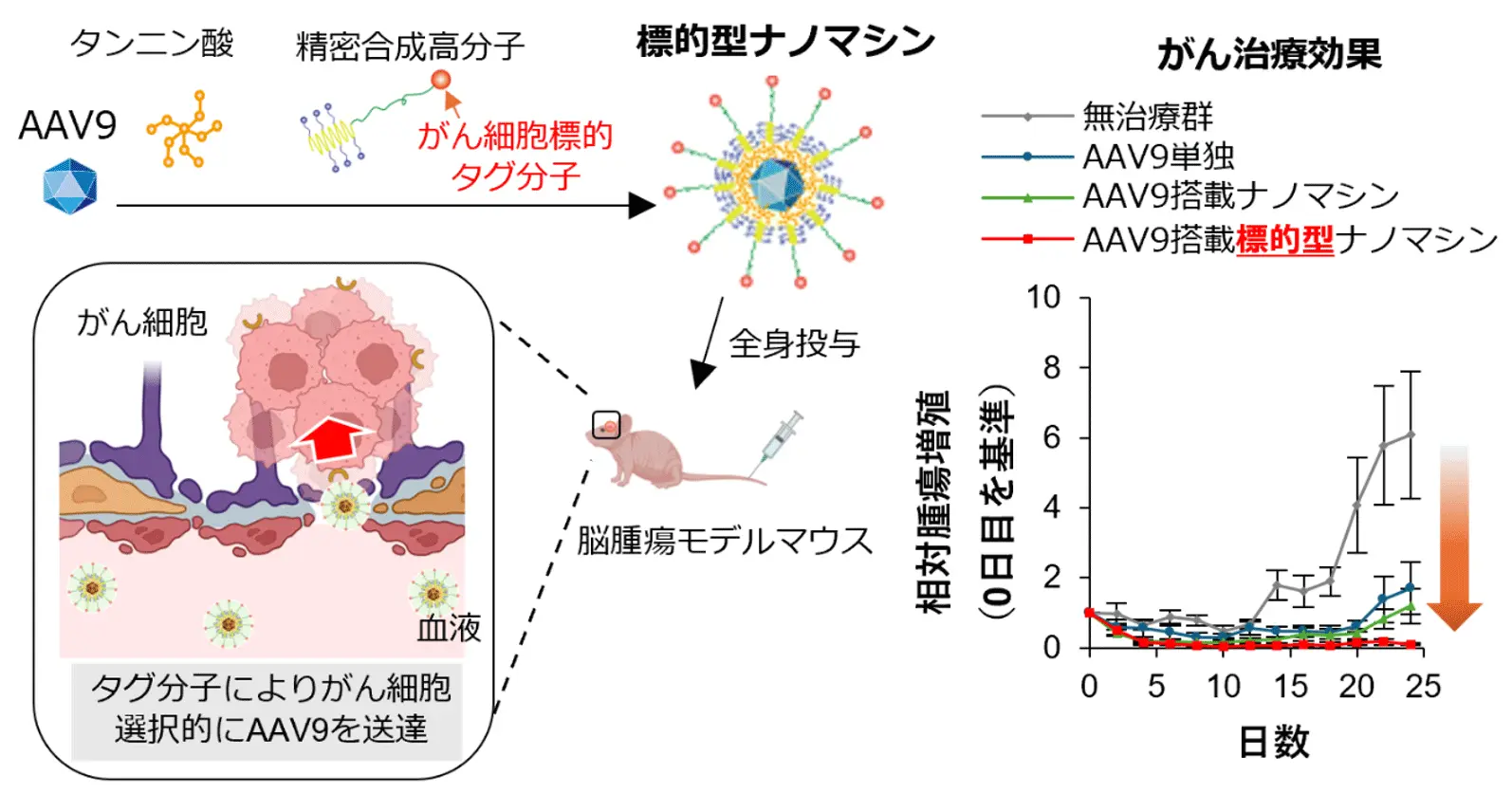
AAVをがん細胞選択的に送達するため、本研究グループは、がん細胞表面に多く発現するタンパク質に特異的に結合する環状ペプチド分子[用語5]をタグ(荷札)として用いるAAV搭載標的型ナノマシンを新たに開発しました(図1)。本標的型ナノマシンは、ワインや茶に多く含まれるポリフェノールの一種であるタンニン酸と精密合成高分子を基盤構造とし、環状ペプチドタグ分子により新たにがん細胞標的能が付与されました。
タンニン酸は、疎水性相互作用や水素結合を介してタンパク質やウイルスベクターなどの生体分子と相互作用し、複合体を形成するユニークな特徴を持ちます。この性質を利用し、研究グループはこれまでに、タンニン酸とエステル形成するフェニルボロン酸導入精密合成高分子を組み合わせた生体分子送達ナノマシンを報告しています(Y Honda, et al. ACS Appl. Mater. Interfaces 2021, 13, 54850−54859)。このナノマシンは水中で搭載したい生体分子、タンニン酸、精密合成高分子を混合するだけで簡単に形成され、細胞内の酸性環境で搭載分子を放出します。またこのナノマシンにAAVを搭載することで、AAVの活性を損なうことなく体内での中和抗体の影響を回避できることも報告しています(Y Honda, N Matsudaira, et al. ACS Nano 2025, 19, 7690-7706)。そこで研究グループは、AAV搭載ナノマシンにがん細胞標的能を付与し、効率的かつ安全性の高いAAVがん遺伝子治療の実現を図りました。
悪性度が高く治療の選択肢が少ない脳腫瘍のひとつ、膠芽腫を脳に同所移植したがんモデルマウスにAAVセロタイプ9型(AAV9)を搭載した本標的型ナノマシンを注射投与すると、AAV9単独や非標的型ナノマシンと比較して、AAV9のがんへの集積が約2-3倍に増加しました。また肝臓や腎臓など正常組織への集積はAAV9単独と比較して約70%抑制され、がんへの高い選択性が示されました。また、がん治療遺伝子を組み込んだ治療用AAV9を搭載すると、従来の3分の1の投与量で十分な治療効果を示し、肝毒性をAAV9非投与マウスと同程度にまで有意に抑制することに成功しました。これらの結果は、本標的型ナノマシンが、AAVによるがん治療の大きな課題であったがんへの不十分な集積と高容量投与による肝毒性という課題を克服し、画期的なAAV送達システムとして非常に有用であることを示唆しています。
尚、動物実験には純系マウスを使用し、iCONM 動物実験委員会が承認した研究計画書に則って実施しました。
用語説明
- [用語1]
- アデノ随伴ウイルスベクター(AAV):分裂細胞および非分裂細胞への効率な遺伝子導入が可能であり、これら標的細胞では遺伝子発現が長期間持続することから、遺伝子治療用ベクターとして臨床応用されている。
- [用語2]
- ナノマシン:近年、1〜100 nm程度の粒子径を持つ微小な粒子であるナノ粒子を用いた医療への応用が多数開発され、特に、薬剤送達システム(ドラッグデリバリーシステム、DDS)と呼ばれる薬剤を体内で運搬する担体として注目が集まっている。薬や核酸の効果を上げ、副作用を減らすために、ターゲットとなる細胞や組織に効率的に薬を到達させ、必要量をタイミングよく放出させるシステムで、ナノ粒子を用いたDDSを「ナノDDS」あるいは、高機能化されたものを「ナノマシン」と呼称することがある。
- [用語3]
- タンニン酸(Tannic Acid):赤ワインや茶などに多く含まれる、植物由来のポリフェノール化合物の一種である。疎水性相互作用や水素結合を介して、タンパク質などの様々な生体分子と結合して複合体を形成する。
- [用語4]
- カプシド :ウイルスの遺伝物質(DNA、 RNA)を包んで保護する殻。
- [用語5]
- 環状ペプチド分子:高い結合特異性と安定性を持つ小型のペプチドで、がん細胞表面の特定分子を高精度に認識できる。
論文情報
- 掲載誌:
- Journal of Controlled Release
- タイトル:
- Tumor-targeted adeno associated virus-loaded complexes comprising tannic acid and phenylboronic acid-polymers for orthotopic glioblastoma therapy
- 著者:
- Nozomi Matsudaira, Yuto Honda, Hiroaki Kinoh, Xueying Liu, Shuhei Nagao, Shoko Matsutomo-Nitta, Guo Haochen, Hiromi Hayashita-Kinoh, Miho Aizawa, Kyohei Muguruma, Yutaka Miura, Atushi Shishido, Takashi Okada, Nobuhiro Nishiyama
Journal of Controlled Release誌について
Journal of Controlled Release(JCR)は、ドラッグデリバリーシステム(Drug Delivery Systems)、製剤学、ナノメディシン、生体材料、薬物動態、遺伝子デリバリーなどの分野を専門とする、Elsevier が発行するドラッグデリバリー分野の査読付き学術誌です。直近のインパクトファクター(IF)は 10.1。ISSN: 0168-3659(Print)、1873-4995(Web)。年間発行数は 24号。
公益財団法人川崎市産業振興財団について
産業の空洞化と需要構造の変化に対処する目的で、川崎市の100%出捐により昭和63年に設立されました。市場開拓、研究開発型企業への脱皮、それを支える技術力の養成、人材の育成、市場ニーズの把握等をより高次に実現するため、川崎市産業振興会館の機能を活用し、地域産業情報の交流促進、研究開発機構の創設による技術の高度化と企業交流、研修会等による創造性豊かな人材の育成、展示事業による販路拡大等の事業を推進し、地域経済の活性化に寄与しています。
ナノ医療イノベーションセンターについて
川崎市川崎区殿町の国際戦略拠点(キングスカイフロント)におけるライフサイエンス分野の拠点形成の核となる先導的な施設として、文部科学省より「地域資源等を活用した産学連携による国際科学イノベーション拠点整備事業」の支援を受け、川崎市、公益財団法人川崎市産業振興財団が整備を進め、2015 年 4 月に運営を開始した研究センターです。産学官が1つ屋根の下に集い、異分野融合体制で革新的課題の研究および研究成果の実用化に取り組んでいます。片岡一則センター長は、2023 年、英国・クラリベイト社のデータ解析に基づきノーベル賞級の研究成果を創出する研究者を表彰する Citation Laureates™(引用栄誉賞)に選出されました。
東京科学大学 総合研究院 化学生命科学研究所について
「分子を基盤とする化学および生命化学に関する基礎から応用までの研究の深化、発展を通じて、新しい学理の創成と次世代科学技術の創出を実現し、人類の高度な文明の進化と、より豊かで持続的な社会の具現化に貢献する」というミッションを掲げています。本研究所では、分子を基盤とし、新しい研究アプローチも取り込みながら、応用化学と生命科学の2分野において、世界を先導する研究を生み出しています。
東京大学医科学研究所 遺伝子・細胞治療センター 分子遺伝医学分野について
ウイルスベクターに関する独自の技術を応用した遺伝子・細胞治療の研究を推進しています。特にアデノ随伴ウイルスベクターに関し、次世代の製造・精製技術や、ドラッグデリバリーシステムに関する技術開発を行っています。また、神経・筋疾患およびがんの分子病態解析を推進しており、遺伝子・細胞治療における様々な課題を解決する新規治療法の開発を目標としています。
関連リンク
東京科学大学 総務企画部 広報課
- media@adm.isct.ac.jp
- Tel
- 03-5734-2975
- FAX
- 03-5734-3661