ポイント
- メッセンジャーRNA (mRNA)を用いて緑膿菌に対する抗体を体の中で作り出す、次世代抗体治療を開発しました。
- 緑膿菌は「針」を使ってヒト細胞に毒素を注入して攻撃しますが、この針に蓋をする抗体を作るmRNAを設計しました。
- この抗体を小型化することで、緑膿菌が感染した肺に抗体を効率よく送達でき、マウスにおいて治療効果が向上しました。
- 臨床では多剤耐性を持つ緑膿菌が免疫力の低下した患者へ感染することが問題となっていますが、その状況を模倣したモデルにおいても治療に成功しました。
- 緑膿菌に留まらず、今後世界的脅威となる様々な薬剤耐性菌に対して、画期的な治療法となります。
- 分子シミュレーションで、抗体が毒素から細胞を守るメカニズムを解明しました。
概要
本研究は、京都府立医科大学大学院医学研究科 麻酔科学 助教 木下真央、同大学附属病院 病院長 佐和貞治、東京科学大学総合研究院難治疾患研究所 先端ナノ医工学分野 教授 内田智士らの共同研究であり、科学雑誌『Nature Communications 』に(2026年4月9日)付けでオンライン掲載されましたのでお知らせします。
背景
現在、多くの薬(抗菌薬)が効かない「薬剤耐性菌」が世界中で増えており、大きな問題になっています。2050年までにその死者数が、がんの死者数を超えてしまうと予測されるほど深刻です。特に緑膿菌は、WHO(世界保健機関)からも最も警戒すべき病原体の一つに指定されています。主に免疫力の低下した人に感染し、肺炎や尿路感染により死に至ることもありますが、抗菌薬が効かないことが多く、新しい治療法の開発が強く求められています。
これに対し、私たちの研究チームは、細菌が毒素を送り込む「注射器」の仕組みをブロックする「抗体[用語1]」という武器を作ってきました。しかし、この武器を作るには、手間もコストもかかるという課題がありました。
そこで今回、新型コロナワクチンでも使われたメッセンジャーRNA(mRNA[用語2])の技術を応用しました。この方法は、「武器の設計図」を体に送り込み、自分の体の中で武器を作らせる仕組みです。これにより、安価で迅速かつ効率的に治療薬を作ることが可能になります。
本研究で、薬が効かない強力な細菌に感染したマウスに対してこの新しい治療を行ったところ、生存率が劇的に向上しました。この成果は、将来、薬の効かない細菌から多くの命を救うための、画期的な一歩になると期待できます。
研究成果
1. 抗体mRNA治療の概要
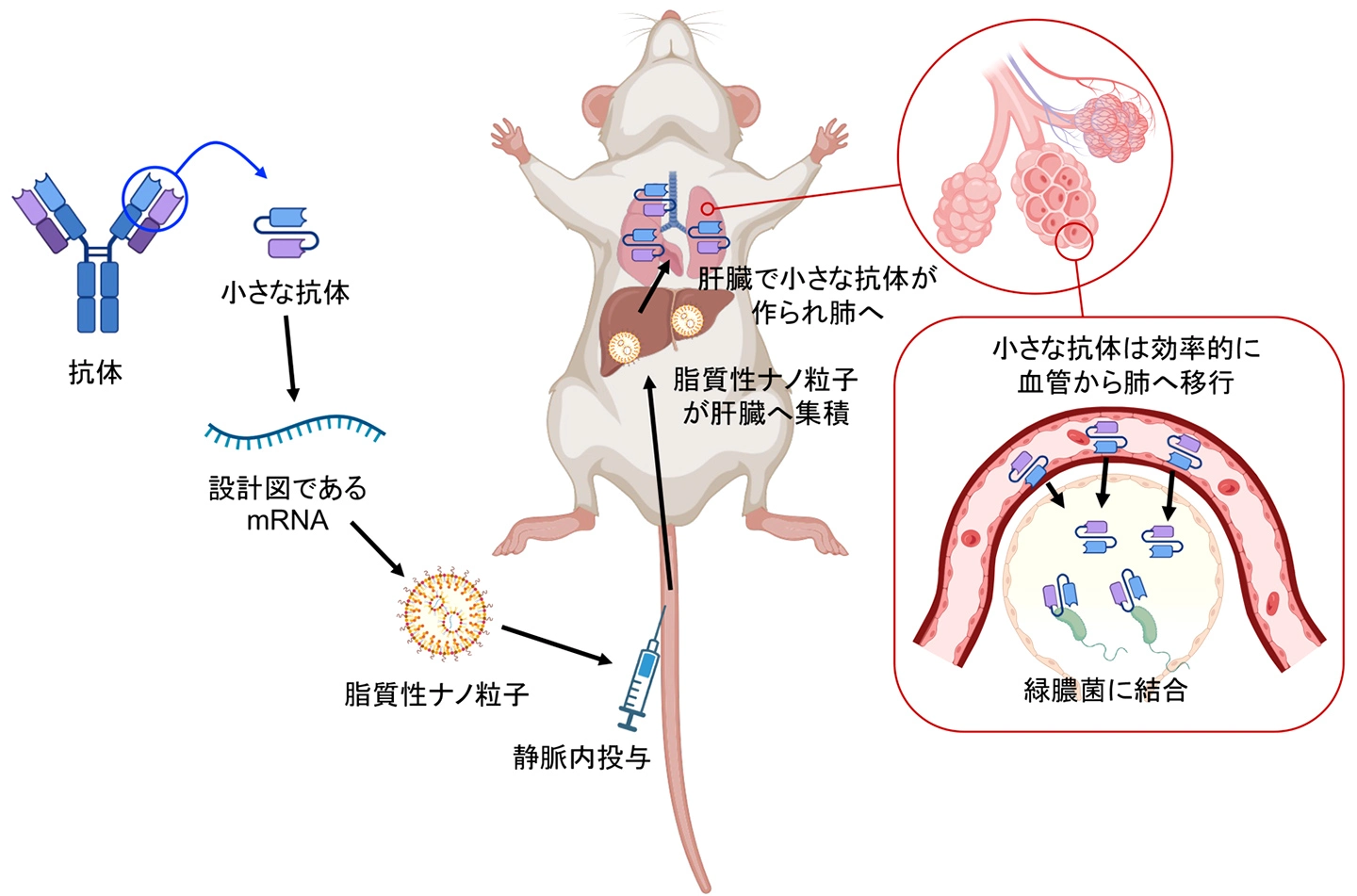
図1は、戦略の概要を示しています。まず、「武器」である抗体は、標的の分子に結合する部分と、構造の基盤となる部分からなりますが、今回、標的に結合する部分だけからなる小さな抗体(単鎖抗体)を設計しました。「武器の形をコンパクトに」することで、細菌が暴れている肺の奥深くまで武器を届きやすくする狙いです。しかし、この小さな抗体は、そのまま体内に投与しても数十分程度で排泄されてしまうため、薬として使うことはできません。一方で、その設計図となるmRNAを投与すると、体の中で数日間にわたって小さな抗体を作り続けることができ、その間、効果が持続します。実際には、このmRNAを脂質性ナノ粒子と呼ばれる小さなカプセルに包んで投与すると、肝臓へ集まり、そこで小さな抗体が作られます。この小さな抗体は血流に乗って、緑膿菌が感染した肺へと到達し、緑膿菌の攻撃から肺の細胞を守ります。
2. 抗体が緑膿菌の毒素から細胞を守る仕組みの解明
図2Aに示すように、緑膿菌は針のような構造を持つIII型分泌装置を用いて、肺の様々な細胞に毒素を送り込みます。抗体はこの「針装置」の先端にあるタンパク質であるPcrVに結合して蓋をすることで、細胞に対する毒素の注入を防ぎます。このことで緑膿菌による肺組織の破壊や肺での増殖が抑制されます。
具体的には、PcrVは5つ集まった5量体構造として針装置の最先端を形成し、細胞へ毒素を送り込むための通り道において、毒素の通過をコントロールしています(図2A)。これに対し、抗体はPcrVに結合することで、毒素の注入をブロックすると考えられます。
これまで、図2Bのように、PcrVの5量体に対し1分子の抗体が結合していると考えられていました。PcrVが形成する中心の孔の近くに抗体が位置しており、これにより毒素の注入を防いでいると想定されます。一方、今回、図2Cのように、PcrVの5量体に対し2分子の抗体が結合できることが、分子シミュレーション及び実験により明らかになりました。2分子の抗体が結合することでより強力に機能が発揮された可能性があります。
図2Dは、AlphaFold3[用語3]を用いて、より高精度に結合構造を予測したものです。抗体がPcrVに対して鍵と鍵穴のようにと密接に結合し、その中心の孔を覆う様子がみてとれます。このことで、毒素の細胞への注入を防いでいるのではないかと考えられます。
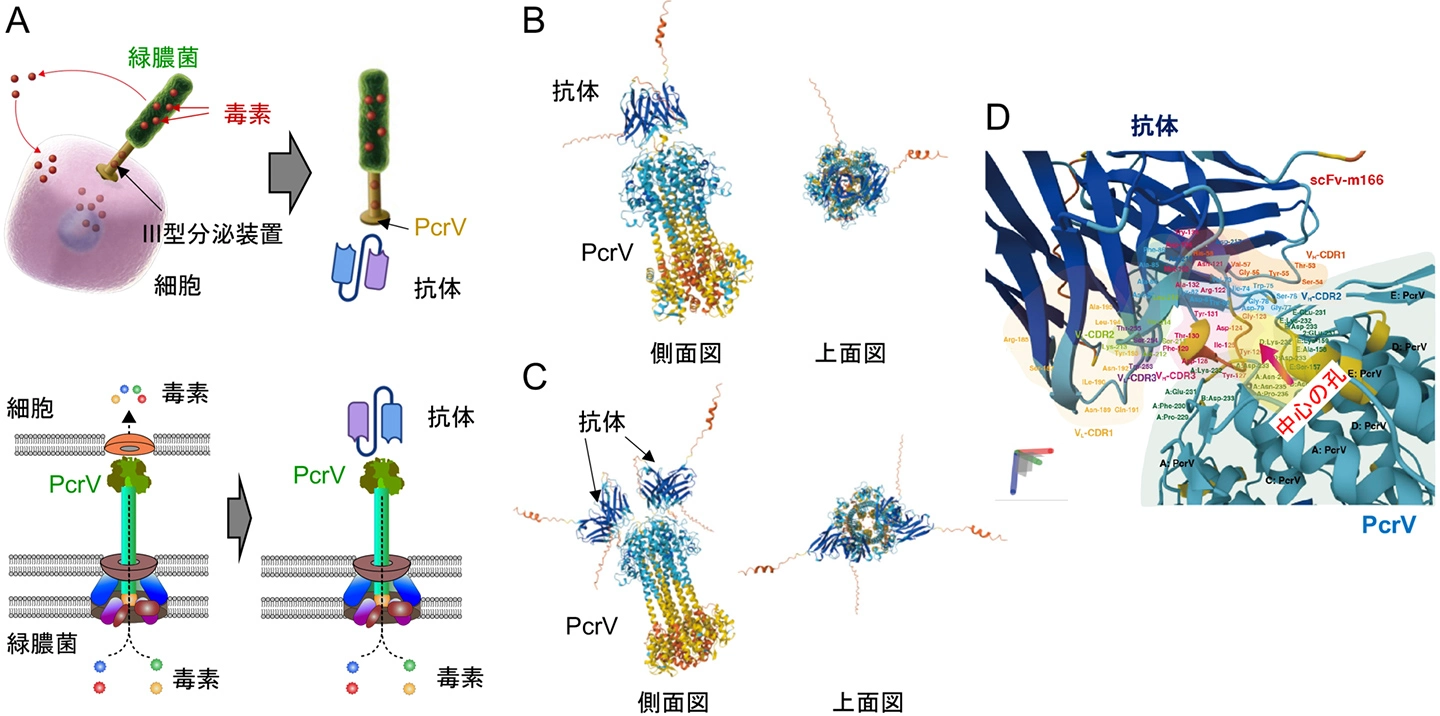
A. 概念図。緑膿菌はIII型分泌装置を用いて、細胞に毒素を注入する。抗体はIII型分泌装置の先端のPcrVに結合して、毒素の注入をブロックする。
B. PcrVに1分子の抗体が結合するモデル。C. PcrVに2分子の抗体が結合するモデル。D. AlphaFold3を用いた高精度な構造予測。
3. 小さい抗体のmRNAを用いて、マウス緑膿菌肺炎治療に成功
次に、小さな抗体を体の中で作るmRNAを用いた治療を行いました。まず、正常マウスの肺に緑膿菌の株を感染させ、30分後にmRNA治療を行いました(図3A)。図3Bに示すように、mRNAを投与しない場合、1日後には全てのマウスが死亡しました。一方で、mRNAを投与した群では1週間後に8割のマウスが生存し、高い治療効果を認めました。
臨床現場では、多剤耐性を持つ緑膿菌が免疫力の低下した患者へ感染することが問題となります。そこでその状況を模倣し、患者から単離された多剤耐性かつ高細胞毒性の緑膿菌株を、免疫不全マウスに対して投与しました。すると、未治療では3日間で全てのマウスが死亡するのに対して、mRNAを用いて治療すると1週間後も半分近くのマウスが生存しており、優れた治療効果が確認されました(図3C)。また、ここで用いた株に感受性を持つ抗菌薬(コリスチン)を用いて治療しても生存率は2割以下でした。すなわち、mRNA抗体治療は、既存の抗菌薬治療を上回る高い効果を示しました。
また、本治療を臨床応用する際、既存の抗菌薬との併用が想定されます。そこでその併用を試したところ、全てのマウスが1週間後も生存するという極めて高い治療効果が得られました(図3C)。このように、抗体mRNA治療は、既存の抗菌薬治療を補完する補助療法(アジュバント治療)としても有望です。
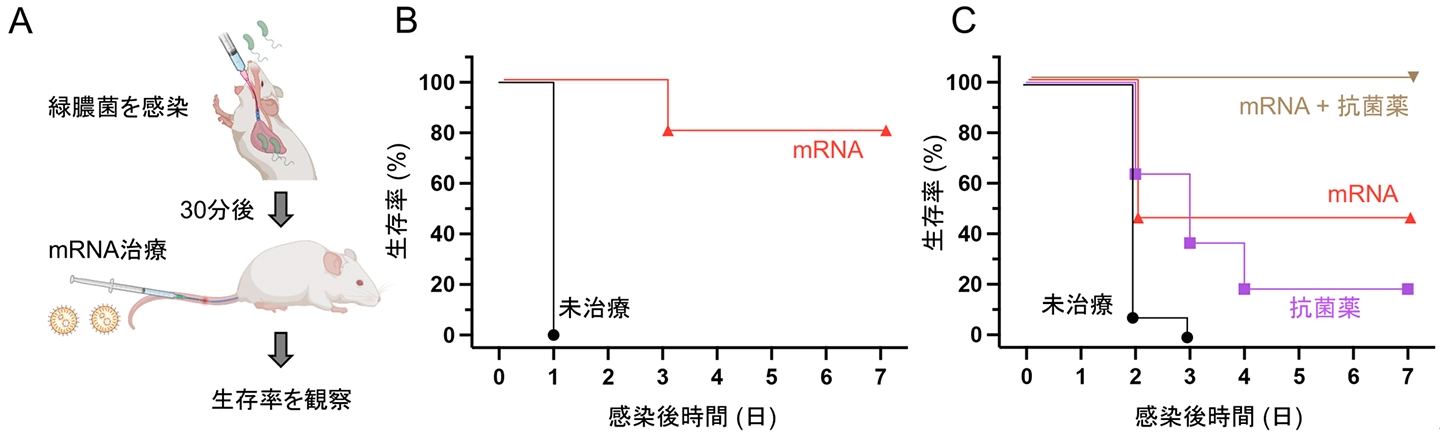
A. 実験の概要。B. 正常マウスの感染モデルにおける生存率。C. 免疫不全マウスに、多剤耐性かつ強毒性の緑膿菌を感染させた際の生存率。
抗体治療のメカニズムの解析も行っており、mRNA治療により肺での緑膿菌の増殖が抑えられること(図4A)、肺炎が軽減すること(図B)などが明らかとなりました。図4Bでは、未治療の場合、肺に炎症細胞が広範囲に浸潤しているのに対して、mRNA治療を行うとほとんど炎症が観察されませんでした。
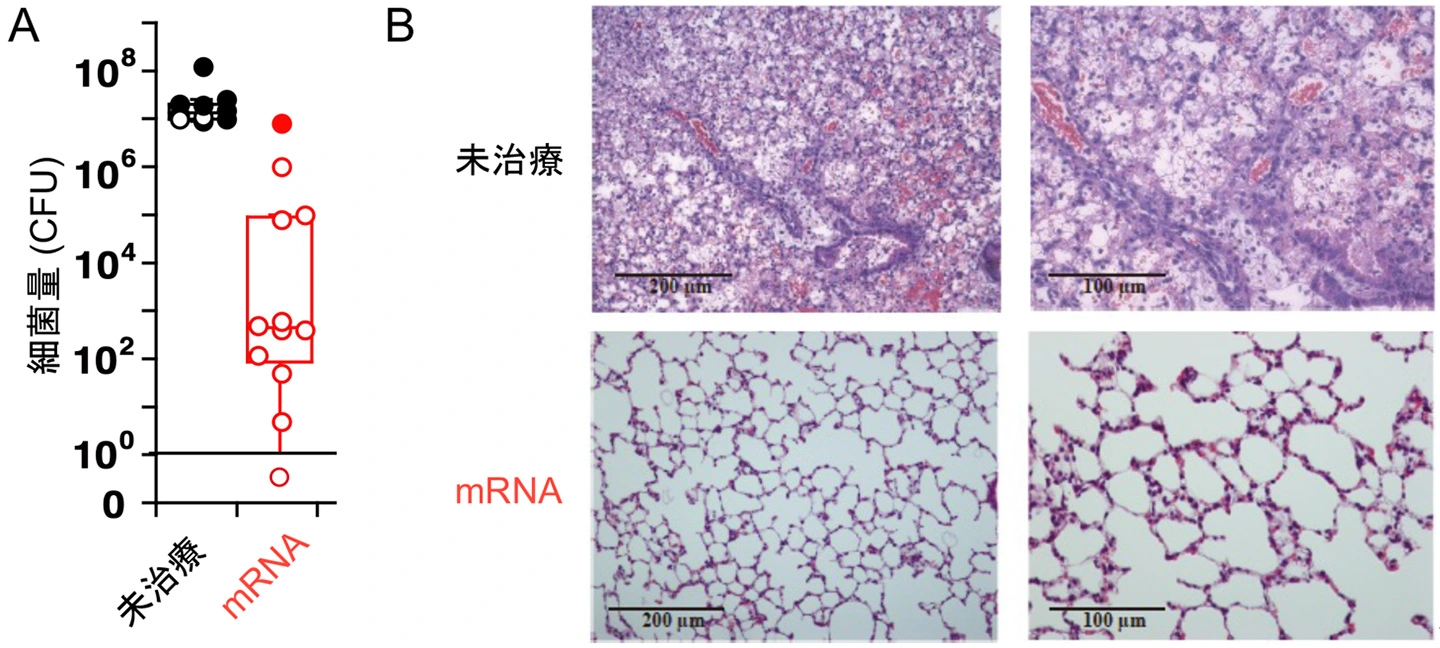
A. 肺における緑膿菌の量。B. 感染後の肺。
今回、肺組織へ効率的に抗体を送り届けるため、小さな抗体を設計しました。抗体を小型化したことの効果を調べるため、通常の抗体と同程度の大きさを持つ抗体の設計図であるmRNAの投与も行いました。複数のモデルで抗体の大きさの治療効果に対する影響を調べたところ、いずれにおいても小さな抗体がより高い生存率を示しました(図5A、B)。そのメカニズムについて、小さな抗体の方が通常サイズの抗体と比べて、肺の上皮側(緑膿菌が感染する部分)により効率的に送達されていることが明らかとなりました(図5C)。
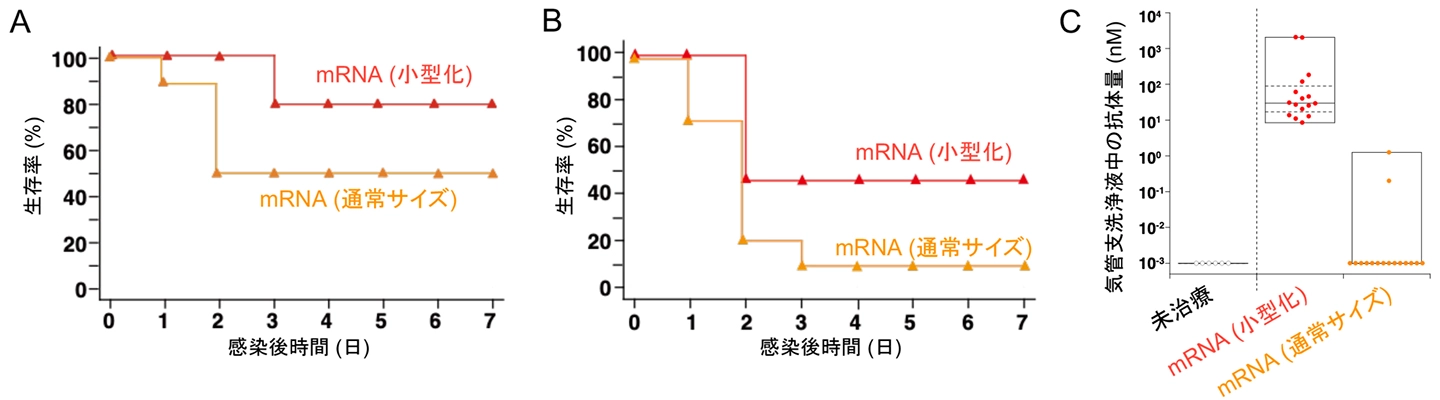
A. 正常マウスの感染モデルにおける生存率。B. 免疫不全マウスに、多剤耐性かつ強毒性の緑膿菌を感染させた際の生存率。C. 肺の上皮側(感染が起こる部位)における抗体の量。
4. 本研究の画期的な点
-
多剤耐性菌に対するmRNA抗体治療
抗体医薬はがん治療をはじめとした様々な医療領域で応用されていますが、感染症領域ではコストの問題で実用化が進んでいません。この課題に対して、本研究では、mRNAを用いた抗体治療の可能性を示しました。今後mRNAを用いることで抗体治療を低コスト化することができれば、感染症領域での応用が期待されます。人類の健康上の大きな脅威となる多剤耐性菌への対策としても、期待されます。 -
抗体の小型化
これまでも抗体mRNA治療の報告はありましたが、主に通常の抗体と同様の設計が行われていました。今回、抗体を小型化することの有用性を世界に先駆けて報告しました。小型化抗体は速やかに排泄されるため、そのままの形で薬にすることは困難でしたが、mRNAを用いて体内で持続的に作らせることで、はじめて治療応用が可能になりました。 -
臨床を模倣したモデル
臨床では多剤耐性を持つ緑膿菌が免疫力の低下した患者へ感染することが問題となっています。今回、その状況を模倣したモデルにおいても治療に成功しました。臨床応用に直結する成果であり、今後の開発の大きな推進力となります。 -
抗体機能の分子機構の解明
AlphaFold3を用いた高精度な構造予測によって、緑膿菌が細胞に毒素を注入する針構造の先端の穴の部分を覆うように抗体が結合し、毒素の注入を阻害している可能性が示されました。このような知見は、同様の戦略を他の感染症へと展開するための有力な基盤となります。
今後の展開
- 世界的な脅威である多剤耐性菌の問題に対し、本研究ではmRNAを用いた次世代抗体治療を確立しました。細菌の毒素注入装置を直接無力化するという革新的なアプローチにより、2050年に予測される多剤耐性菌による深刻な被害を防ぐ決定打となることが期待されます。
- mRNA技術を応用することで、抗体を小型化しても十分な期間効果を得ることに成功しました。また、従来の抗体薬と比べて大幅にコストを下げ、安定して供給できることが期待されます。mRNAが新型コロナウイルスワクチンとして実用化され世界中で接種されているという実績は、本研究のようなmRNAを用いた創薬を大きく後押しします。
- 今回の成果は緑膿菌のみならず、同様の毒素機構を持つサルモネラ菌や赤痢菌といった他の病原菌への応用も容易です。また、臨床を模倣したモデルにおいて得られた優れた延命効果に関するデータは、今後の臨床応用に向けた開発の強い推進力となります。
- 今後は、免疫不全や重症肺炎に苦しむ患者に対しても迅速かつ安全に抗体を供給できる「次世代の医療インフラ」としての普及を目指し、高価な抗体治療を誰もが受けられる身近なものへと変える、医療のデジタルトランスフォーメーションを推進します。
用語説明
- [用語1]
- 抗体:体内に侵入した病原体などの異物に結合して、それを排除する役割を持つタンパク質です。近年、それを薬として用いる抗体医薬が臨床応用されていますが、コストの問題から感染症への応用はあまり進んでいません。
- [用語2]
- mRNA:細胞の中でタンパク質を作るための設計図となる物質です。新型コロナウイルスワクチンでは、ウイルスのタンパク質を体の中で作らせることで、それに対する免疫を誘導しています。本研究では、抗体を作らせることで、緑膿菌の治療に用いています。mRNAは新型コロナウイルスワクチンとして実用化されたことを契機に、現在、その医療応用が加速しています。2023年ノーベル生理学・医学賞の受賞対象となりました。
- [用語3]
- AlphaFold3:Google DeepMindが開発したタンパク質の構造を高精度に予測する技術です。2024年ノーベル化学賞の受賞対象となり、生体分子の相互作用予測に革新をもたらしました。
論文情報
- 掲載誌:
- Nature Communications
- タイトル:
- Fc-Free Single-Chain Antibody mRNA Therapy for Airway Infection of Multidrug-Resistant Pseudomonas aeruginosa
- 著者:
- Mao Kinoshita, Ken Kawaguchi, Yuki Mochida, Nguyen B. T. Le, Atsushi Kainuma, Naoko Takeda-Miyata, Motohiro Kojima, Teiji Sawa & Satoshi Uchida