ポイント
- ノロウイルス主要流行株GII.4と新興株GII.17に対するモノクローナル抗体を作製
- IgM抗体は10本のFabを活用し、抗原密度が高いウイルス粒子表面で最大100倍の結合強化を示すことを定量化
- 多価性による「アビディティ効果」を定量的に解明し、次世代ワクチン・抗体医薬の設計に新たな戦略を提供
概要
東京科学大学(ScienceTokyo) 物質理工学院 材料系の田川純平大学院生(博士後期課程)と総合研究院 フロンティア材料研究所の谷中冴子准教授らの研究チームは、世界的に流行するノロウイルス[用語1]の主要株GII.4と、新興株GII.17に対するモノクローナル抗体を作製し、ウイルスとの結合メカニズムを分子レベルで解明しました。
ノロウイルスは年間約7億件の感染を引き起こし、医療・社会コストは600億ドル規模に達する深刻な公衆衛生課題です。既存の抗体やワクチンは、ウイルスの多様な変異に対応することが難しく、より強力で広域に作用する抗体設計が求められていました。
本研究では、IgM抗体[用語2]が持つ10本のFab[用語3]による「多価性」[用語4]に着目し、その結合強化の仕組みを世界で初めて定量的に示しました。高速原子間力顕微鏡(HS-AFM[用語5])により、IgM抗体がウイルス様粒子表面を“スキャン”しながら多点で結合する様子をリアルタイムで可視化するとともに、表面プラズモン共鳴(SPR[用語6])法による相互作用解析で、抗原密度が高い環境ではIgMの結合力が最大100倍に増強されることを明らかにしました。この「アビディティ効果」[用語7]は、Fab単体とウイルスの親和性が低くても、複数の結合点を同時に利用することでIgG抗体[用語8]に匹敵する高い結合力を発揮することを示しています。
この成果は、ノロウイルスの変異に強い抗体や次世代ワクチン設計に新しい戦略を提供します。今後は、抗体の構造解析によるエピトープ同定や、広域中和抗体・ワクチンの開発を進め、産学連携による社会実装を目指します。
本成果は、3月12日付(現地時間)の「Protein Science 」誌に掲載されました。
背景
ノロウイルスは世界で年間約7億件の感染を引き起こし、約100万人の入院、21万9千人の死亡をもたらし、医療・社会コストは年間600億ドルに達すると推定されています。特にGII.4系統のウイルスは過去20年以上にわたり世界的な流行株として猛威を振るい、最も対策すべき病原体の1つです。特に、2014年冬に急速に拡散した新興株GII.17は、従来のGII.4を凌ぐ感染力を持っています。
ノロウイルスはRNAウイルスに分類され、外殻は180個のカプシドタンパク質からなる高密度構造を持ちます。この構造は免疫系にとって複雑な標的であり、抗体による中和は容易ではありません。既存のワクチンや抗体医薬は、ウイルスの多様な変異や抗原性の違いに対応することが難しく、広域に作用する抗体設計が求められています。
従来の研究ではIgG抗体が中心に解析されてきましたが、IgM抗体は10本の抗原結合部位(Fab)を持つ多価構造により、理論的には高い結合力を発揮できると考えられていました。しかし、そのメカニズムを定量的に示した研究はほとんどありませんでした。
研究成果
本研究では、ノロウイルスの主要流行株GII.4と新興株GII.17に対するモノクローナル抗体を作製し、ウイルスと抗体の結合メカニズムを分子レベルで解明しました。
1. IgM抗体の動的結合を世界初可視化
高速原子間力顕微鏡(HS-AFM)を用いて、IgM抗体がウイルス様粒子表面を"スキャン"しながら結合する様子をリアルタイムで観察しました(図1a)。IgMは10本のFabを持つ多価構造により、ウイルス表面に複数の結合点を形成し、安定した結合を維持することが確認されました。この粒子表面をスキャンしつつ最終的に複数の結合点で安定的結合を維持する「スライディング結合」メカニズムは、ウイルス表面を物理的に覆うことで感染阻害に寄与する可能性があります。
2. 多価性による結合強化を定量的に証明
表面プラズモン共鳴(SPR)解析により、抗体のFab数(多価性)と抗原密度が結合力を劇的に高めることを定量化しました。IgM抗体は、Fab単体の親和性が低くても、10本のFabを同時に使うことで最大100倍の結合強化を示しました。特に、抗原密度が高いウイルス様粒子表面では、IgMの結合力はIgGに匹敵するレベルに達することが明らかになりました(図1b)。
IgM抗体がIgGと異なる結合モードを持ち、複数点を使って「アビディティ効果」によるウイルスへの強い結合を発揮することは、従来のIgG中心の抗体設計とは異なる新しい戦略の可能性が広がることを示します。IgGとは異なる結合モードと多価性を活用することで、ウイルスの変異に強い抗体や、広域に作用するワクチンの開発が可能になると期待されます。
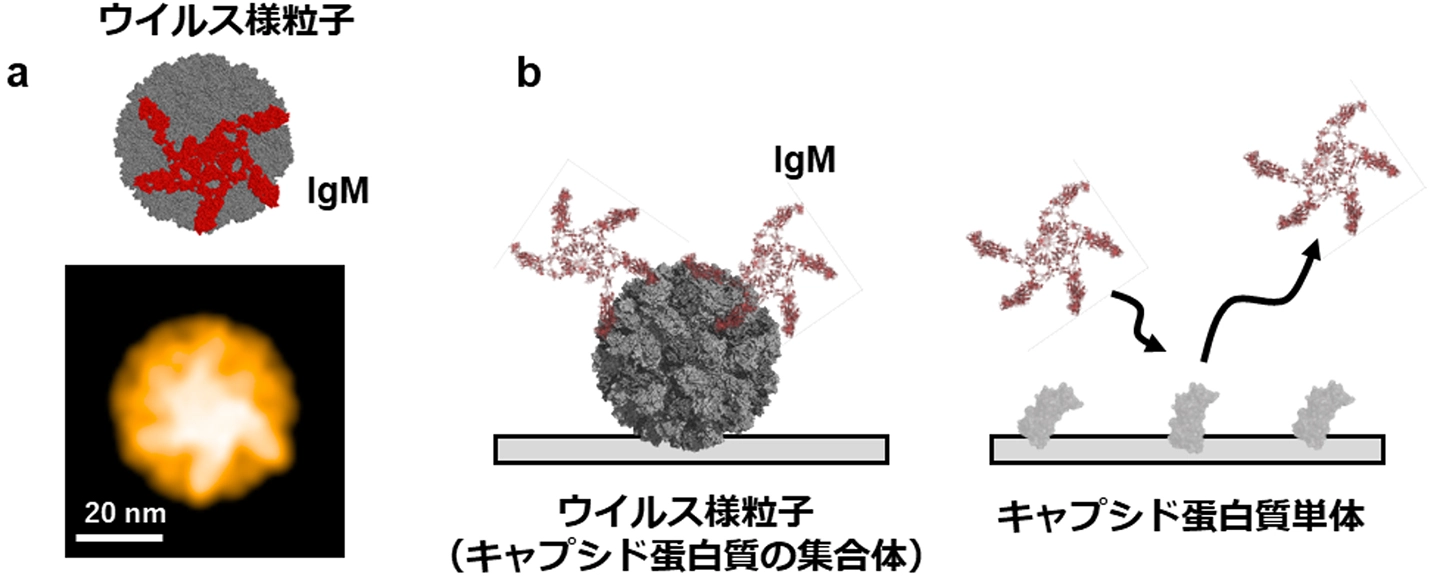
(a)ノロウイルス粒子とIgMの複合体の構造モデルと高速原子間力顕微鏡計測による像
(b)IgMの多価の腕がウイルス様粒子上に高密度で存在するキャプシド蛋白質を効率的に認識している。キャプシド蛋白質単体では効率的に認識されない。
社会的インパクト
ノロウイルスは社会に深刻な負担を与えており、特に高齢者施設や病院、学校などでの集団感染は、医療体制や社会生活に大きな影響を及ぼします。それに対して、本研究は、従来の抗体医薬やワクチン設計の限界を打破し、ノロウイルス感染対策に向けた可能性を示しました。IgM抗体の「多価性」を活用することで、ウイルスの変異に強く、広域に作用する抗体やワクチンの開発が期待されます。これは、パンデミックや季節性流行に対する迅速な対応策となり、感染症対策の新しいパラダイムを提供します。
さらに、この知見はノロウイルスに限らず、インフルエンザや新興ウイルスなど、構造的に類似した高密度抗原を持つ病原体への応用も可能です。結果として、世界的な公衆衛生の改善、医療コストの削減、社会の安定に大きく貢献することが期待されます。
今後の展開
今回の研究で明らかになったIgM抗体の多価性による結合強化は、抗体医薬やワクチン開発に新しい設計指針をもたらします。今後は、抗体がどの部位でウイルスに結合しているのかを構造解析で詳細に解明し、その知見をもとに、複数の変異株に対応できる広域中和抗体の開発を進めます。また、この戦略をワクチン設計に応用し、より強力で長期的な免疫応答を誘導する次世代ワクチンの開発を目指します。さらに、製薬企業や公的研究機関と連携し、臨床試験や製品化に向けた取り組みを加速させ、医療現場や高齢者施設でのノロウイルス感染対策に直結する技術として社会実装を目指します。
付記
本研究は以下の支援を受けて実施されました。
- 国立研究開発法人日本医療研究開発機構(AMED)(SCARDA JP233fa827004、JP21ae0121020、JP23ak0101209)
- 文部科学省/日本学術振興会 科学研究費助成事業(JP22H02755、JP25H02252、20H03228)
- 共同利用・共同研究システム形成事業~学際領域展開ハブ形成プログラム~(CURE)(JPMXP1323015482)
- 生命創成探究センター共同研究(ExCELLSプログラム 23EXC312、24EXC341)
- AMED 創薬等先端技術支援基盤プラットフォーム(BINDS)(JP23ama121031)
- 科学技術振興機構(JST) SPRING(助成番号 JPMJSP2180)
用語説明
- [用語1]
- ノロウイルス(Norovirus):世界的に流行するウイルス性胃腸炎の原因ウイルス。年間約7億件の感染を引き起こし、嘔吐や下痢などの症状を伴う。
- [用語2]
- IgM抗体(Immunoglobulin M):免疫応答の初期に産生される抗体。10本のFab(抗原結合部位)を持つ多価構造により、複数の抗原に同時に結合できる。
- [用語3]
- Fab(Fragment antigen-binding):抗体の抗原結合部位。抗体がウイルスや細菌などの抗原を認識するための構造。
- [用語4]
- 多価性(Multivalency):1つの抗体分子が複数の抗原結合部位を持つ性質。IgMは10本のFabを持ち、IgGは2本。
- [用語5]
- 高速原子間力顕微鏡(High-Speed Atomic Force Microscopy, HS-AFM):ナノスケールで分子の動きをリアルタイム観察できる顕微鏡技術。
- [用語6]
- 表面プラズモン共鳴(Surface Plasmon Resonance, SPR)法:抗原と抗体の結合強度をリアルタイムで測定する分析技術。
- [用語7]
- アビディティ効果(Avidity Effect):複数の結合部位を同時に使うことで、全体として非常に強い結合力を発揮する現象。
- [用語8]
- IgG抗体(Immunoglobulin G):免疫応答の後期に産生される抗体。Fabは2本で、IgMに比べて単価性だが、親和性が高い。
論文情報
- 掲載誌:
- Protein Science
- タイトル:
- Characterization of high affinity IgM and IgG monoclonal antibodies against norovirus variants GII.4 and GII.17
- 著者:
- Jumpei Tagawa, Saeko Yanaka*, Yuri Kato, Akitsu Masuda, Jae Man Lee, Akinobu Senoo, Kosuke Oyama, Takayuki Uchihashi, Motohiro Nishida, Takahiro Kusakabe, Jose M.M. Caaveiro*(*責任著者)
- DOI:
- 10.1002/pro.70522
研究者プロフィール
田川 純平 Jumpei Tagawa
東京科学大学 物質理工学院 材料系 大学院生(博士後期課程)
研究分野:生体分子工学、構造生物学
谷中 冴子 Saeko Yanaka
東京科学大学 総合研究院 フロンティア材料研究所 准教授
研究分野:生体分子工学、統合構造生物学
カアベイロ・ホセ Jose Caaveiro
九州大学 副理事/大学院薬学研究院 教授
研究分野:生体分子工学、構造生物学
日下部 宜宏 Takahiro Kusakabe
九州大学 大学院農学研究院 教授
研究分野:昆虫、ゲノム生物学
西田 基宏 Motohiro Nishida
九州大学 大学院薬学研究院 教授
研究分野:心循環生理学、分子薬理学
内橋 貴之 Takayuki Uchihashi
名古屋大学 大学院理学研究科 教授
自然科学研究機構 生命創成探究センター 客員教授
研究分野:高速原子間力顕微鏡解析