ポイント
- mRNAを全身投与により脳へ効率よく送達可能な、高分子ベースの新規送達システムを開発
- 高分子の精密設計により、mRNAの「血中安定性」「脳移行性」「細胞内局在制御」を同時に最適化し、脳内タンパク質発現を約10倍に向上
- 脳内で任意の治療用タンパク質を産生できることから、中枢神経系疾患の新たな治療基盤として期待
概要
東京科学大学(Science Tokyo)総合研究院 難治疾患研究所の乗松純平助教(ナノ医療イノベーションセンター(iCONM)客員研究員)、同大学 物質理工学院 材料系の安楽泰孝准教授(iCONM 副主幹研究員)らの研究チームは、メッセンジャーRNA(mRNA)[用語1]を全身投与で効率的に脳内へ送達可能なシステムを開発しました。
mRNA医薬は、細胞内で任意のタンパク質を産生できることから、多様な疾患への応用が期待されています。一方で中枢神経系(CNS)疾患[用語2]においては、mRNAの血中不安定性や、血液脳関門(BBB)[用語3]による脳移行の制限といった問題により、mRNAを非侵襲的に脳へ送達する技術が確立されておらず、創薬の大きな障壁となっていました。
本研究では、独自設計の高分子ナノキャリアにより、mRNAの「血中安定性」「血中から脳への移行」「細胞内での適切な局在」を統合的に制御することで、全身投与によるmRNAの脳への効率的送達を実現しました。その結果、脳以外の臓器への影響を抑制しつつ、脳内での目的タンパク質発現量を初期設計の約10倍に向上させました。本技術は、有効な治療法が限られていたCNS疾患に対する新たな治療基盤としての展開が期待されます。
本成果は、東京科学大学 物質理工学院 材料系の安楽泰孝准教授、水野ローレンス隼斗助教、東京大学 大学院工学系研究科のオラシオ・カブラル教授、東京科学大学 総合研究院 難治疾患研究所の内田智士教授、乗松純平助教、ナノ医療イノベーションセンター(iCONM)の福島重人副主幹研究員らによって行われ、4月13日付の米国化学会が発行する科学誌「Molecular Pharmaceutics」誌に掲載されました。
背景
アルツハイマー病を始めとする中枢神経系(CNS)疾患は、有効な治療法が限られており、アンメットメディカルニーズ[用語4]の高い疾患として世界的に認識されています。mRNA医薬は、細胞内で任意のタンパク質を発現できることから、CNS疾患を含めた多様な疾患への応用が期待されています。しかしCNS疾患に対する治療では全身投与による非侵襲的アプローチが望まれるものの、mRNAは血中で不安定であることに加え、血液脳関門(BBB)により脳への移行が大きく制限されることが、実用化に向けた大きな障壁となっていました。
研究成果
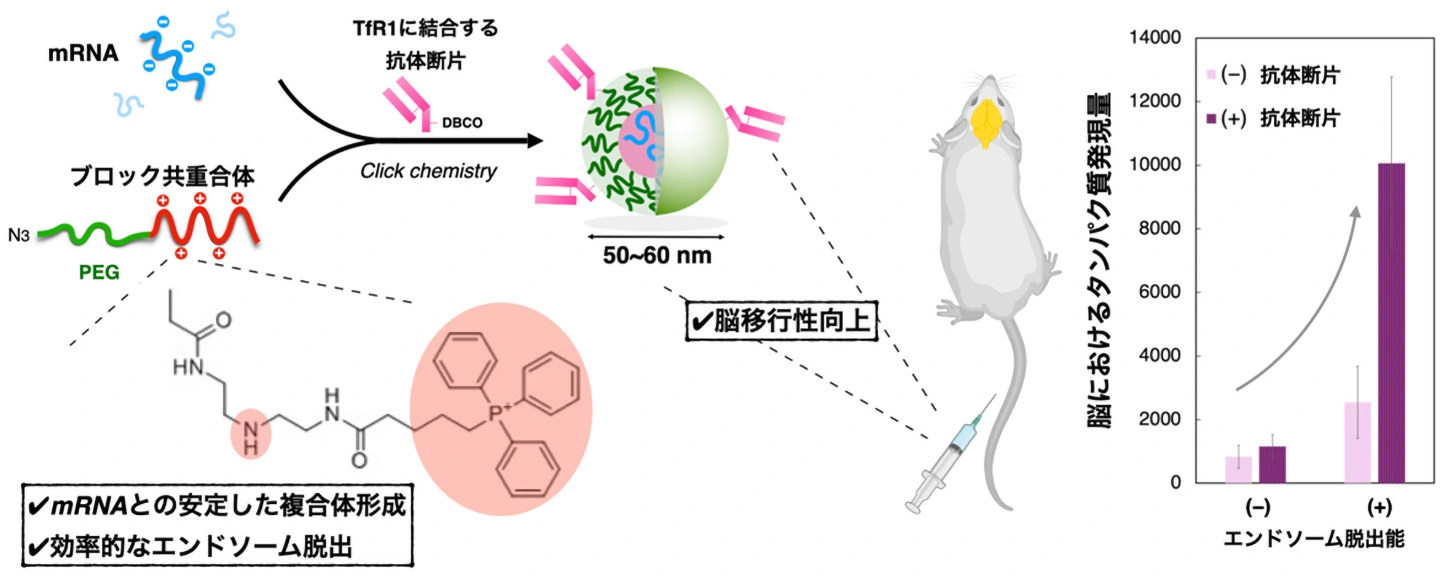
本研究では、全身投与による脳へのmRNA送達に向けて、新規高分子材料を基盤としたナノサイズのmRNA輸送キャリアを構築しました(図1)。具体的には、生体適合性の高いポリエチレングリコールとカチオン性セグメントからなるブロック共重合体[用語5]と、アニオン性のmRNAを、静電相互作用により複合化することで、mRNAを内包したミセル型ナノ粒子を調製しました。
このミセル型ナノ粒子には、従来のナノ粒子で広く用いられてきたアミン系カチオンに代えて、トリフェニルホスホニウム(TPP)を基盤とするカチオンを導入しました。これにより、静電相互作用に加えて、疎水性相互作用を活用した強固なmRNA結合が可能となり[参考文献1]、血中で分解を受けやすいmRNAの安定性を大幅に向上させました。
さらにこのナノ粒子に、細胞内でのタンパク質発現に重要なエンドソーム脱出[用語6]を促進するため、pH応答性を有する構造も導入しました。その結果、エンドソーム内の酸性環境に応答してポリマーの正電荷が増加し、静電相互作用によりエンドソーム膜の損傷[用語7]が誘導され、mRNAの細胞質移行が促進されました。このナノ粒子を初期設計のナノ粒子と比べると、取り込み量が同程度であるにもかかわらず、タンパク質発現が有意に増加しました。この結果から、効率的なタンパク質発現には、mRNAの細胞質への適切な局在が重要であることが示唆されました。
最後に、血中から脳への移行性向上に向けて、ナノ粒子表面にトランスフェリンレセプター1(TfR1)[用語8]に結合する抗体リガンドを修飾しました。断片化抗体を用いることで、粒子サイズへの影響を抑えながら修飾量を精密に制御したうえで、マウスへの全身投与後に臓器分布解析を実施したところ、リガンド修飾数に最適値が存在することを見いだしました。最適条件では脳移行性が向上し、エンドソーム脱出能を併せ持つ場合にのみ、脳内でのタンパク質発現が顕著に増加しました。最終的に、初期設計と比較して脳内での発現量を約10倍に向上させることに成功しました(図1)。
以上より、脳内での効率的なタンパク質発現を達成するためには、mRNAの「血中安定性」「血中から脳への移行」「細胞内での適切な局在」を統合的に最適化することが重要であることが示されました。
社会的インパクト
mRNA医薬の応用拡大に向けては、様々な臓器への送達技術の開発が進められてきましたが、実際に効率的な送達が可能な臓器は肝臓や脾臓などに限られていました。今回の研究は、脳へのmRNA送達に必要な「血中安定性」「脳移行性」「細胞内局在制御」という設計指針を示した点で、これまで困難とされてきた中枢神経系への応用に道を拓くものです。さらに、従来主流であった脂質ナノ粒子に、今回開発した高分子を基盤とする新たな輸送キャリアが加わることで、mRNA送達技術が多様化し、幅広い中枢神経系(CNS)疾患に対する治療戦略の拡充につながります。世界的な高齢化が進む中で、CNS疾患の克服は社会的・経済的に喫緊の課題であり、本技術は人々の健康で豊かな生活の実現に大きく貢献することが期待されます。
今後の展開
mRNAは配列設計を変更することで、多様な治療用タンパク質を発現可能とする高い汎用性を有しています。今後は、脳内に送達されたmRNAの局所分布に着目するとともに、本技術を用いて治療用タンパク質をコードしたmRNAを各種中枢神経系(CNS)疾患モデルマウスに適用し、治療効果および安全性の詳細な評価を進める予定です。
付記
本研究は、日本学術振興会(JSPS)科学研究費助成事業(JP23H00545、JP21H05090、JP23K18558、JP21K18310、JP23KJ0601)、国立研究開発法人科学技術振興機構(JST)の JST FOREST Program(JPMJFR2138)、JST-Mirai Program(JPMJMI21G6)、国立研究開発法人日本医療研究開発機構(AMED)の創薬基盤推進研究事業(21483716)、東京工業大学・東京医科歯科大学マッチングファンド、第一三共株式会社との共同研究費などの支援を受けて行われました。
参考文献
- [参考文献1]
- Norimatsu, J.; Mizuno, H. L.; Watanabe, T.; Obara, T.; Nakakido, M.; Tsumoto, K.; Cabral, H.; Kuroda, D.; Anraku, Y. Triphenylphosphonium-modified catiomers enhance in vivo mRNA delivery through stabilized polyion complexation. Materials Horizons 2024, 11 (19), 4711-4721, 10.1039/D4MH00325J. DOI: 10.1039/D4MH00325J.
用語説明
- [用語1]
- メッセンジャーRNA(mRNA):DNAの遺伝情報をもとに細胞内でタンパク質合成の設計図となる核酸分子。
- [用語2]
- 中枢神経系(CNS)疾患:脳や脊髄に生じる疾患の総称。
- [用語3]
- 血液脳関門(BBB):血液から脳への物質移行を制限するバリア機構。
- [用語4]
- アンメットメディカルニーズ:未だ有効な治療法や診断法が確立されていない医療上のニーズ。
- [用語5]
- ブロック共重合体:異なる性質の高分子鎖(ブロック)を連結したポリマー。
- [用語6]
- エンドソーム脱出:細胞内に取り込まれた物質がエンドソームと呼ばれる小胞から細胞質へ移行する過程。
- [用語7]
- エンドソーム膜の損傷:細胞内に取り込まれた物質を隔離するエンドソームの膜が部分的に透過化または破綻する現象。
- [用語8]
- トランスフェリンレセプター1(TfR1):脳血管内皮に高発現する鉄取り込み受容体。
論文情報
- 掲載誌:
- Molecular Pharmaceutics
- タイトル:
- Ionizable Polymeric Micelles Targeting Transferrin Receptor 1 Enhance Systemic mRNA Delivery to the Brain
- 著者:
- Jumpei Norimatsu, Hayato Mizuno, Yuki Mochida, Shigeto Fukushima, Satoshi Uchida, Horacio Cabral, Yasutaka Anraku
研究者プロフィール
安楽 泰孝 Yasutaka Anraku
東京科学大学 物質理工学院 材料系 准教授
川崎市産業振興財団ナノ医療イノベーションセンター 副主幹研究員(兼務)
研究分野:バイオマテリアル、ドラッグデリバリー、血液脳関門
乗松 純平 Jumpei Norimatsu
東京科学大学 総合研究院 難治疾患研究所 助教
研究分野:mRNA、ドラッグデリバリー
関連リンク
東京大学 大学院工学系研究科 広報室
- Tel
- 03-5841-0235
- FAX
- 03-5841-0529
ナノ医療イノベーションセンター・広報担当
- Tel
- 044-589-6326
- FAX
- 044-589-5706