細胞を使うことなく受容体膜タンパク質の人工進化に成功
阻害剤感受性を10倍向上させたGタンパク質共役型受容体「アデノシン2A受容体」の新規変異体を同定し、細胞種特異的なシグナル制御を実現
ポイント
- 従来は困難だったヒト由来Gタンパク質共役型受容体(GPCR)の実験室内人工進化を無細胞タンパク質合成系とナノディスク技術の組み合わせで実現
- 新規「アデノシンA2A受容体(A2AR)」変異体を同定。哺乳動物細胞内で内因性リガンドであるアデノシンへの応答性を保持しながら、阻害剤感受性を10倍以上に向上
- 新規変異体を用いることで、A2ARシグナルを細胞種選択的に制御できることを実証
- 細胞を用いることなく、GPCR変異体ライブラリーサイズを約1兆(1012)規模に拡大可能に
概要
東京科学大学(Science Tokyo)生命理工学院 生命理工学系の深澤元喜修士課程学生(研究当時)、北尾彰朗教授、同大学 地球生命研究所の松浦友亮教授、福永圭佑特任助教(現:宮崎大学 研究・産学地域連携推進機構 テニュアトラック推進室 准教授)、名古屋大学 大学院工学研究科 松岡佑真博士後期課程学生、清中茂樹教授、千葉大学 大学院理学研究院 村田武士教授らの研究チームは、細胞を用いずに膜タンパク質を実験室内で人工進化させる技術を開発し、リガンド結合能が10倍程度向上したヒト由来アデノシン「A2A受容体(A2AR)」の変異体を同定しました。この変異体を用いることで細胞種特異的なシグナル伝達系の制御が可能です。
細胞外のシグナルを細胞内に伝える役割を担う「Gタンパク質共役型受容体(GPCR: G Protein-Coupled Receptor)[用語1]」の機能を改変した変異体を、合理的に設計することは、膜タンパク質の柔軟性・不溶化しやすい特性から難しく、多くの試行錯誤を要します。本研究では、無細胞タンパク質合成系[用語2]とナノディスク技術を組み合わせ、GPCRの1つであるA2ARが機能発現するよう条件を最適化しました。さらに、実験室進化と次世代シーケンサー[用語3]解析を用いて、変異体集団から特定の阻害剤に対する結合能が向上した変異体を同定しました。変異体は、哺乳動物細胞においてシグナル阻害活性が10倍程度向上しており、この分子機構を原子レベルのシミュレーションで明らかにしました。さらに獲得された変異体の特性を利用し、細胞種特異的にGPCRシグナル伝達を抑制可能であることも示しました。
本研究で開発した手法は、約1012種類規模のGPCRライブラリーから目的の機能を持つ変異体をスクリーニング可能とするものであり、創薬やケモジェネティクス[用語4]分野における新規GPCR変異体探索の基盤技術となることが期待されます。
本成果は、3月6日付(現地時間)の「Journal of the American Chemical Society 」誌に掲載されました。
背景
細胞を用いることなく実験室で人工進化を行う方法(in vitro進化分子工学)は、変異と選択を繰り返すことで、抗体や酵素などの可溶性タンパク質の機能を人為的に改変・最適化する技術として発展してきました[参考文献1-2]。リボソームディスプレイ法[用語5][参考文献3]をはじめとするin vitro進化分子工学は、細胞を介さずに大規模な変異体ライブラリーを扱える点で大きな利点を持ちます。一方、膜タンパク質、特にGタンパク質共役型受容体(GPCR)は、無細胞タンパク質合成系では凝集・不溶化しやすく、in vitro進化分子工学への適用は困難でした。そのため、GPCRの機能改変は主として生細胞を用いた実験系に依存してきました[参考文献4-5]。しかし、生細胞系では取り扱える変異体数や選択条件に制約があり、探索可能な変異体空間は制限されていました。
研究成果
GPCRはヒトゲノム中で最大級の受容体ファミリーです。現在承認されている医薬品の約3~4割がGPCRを標的としています。GPCRの1つであるA2ARは神経疾患、免疫疾患、炎症、がん免疫など幅広い疾患領域に関与する重要な創薬標的です[参考文献6]。しかし、特定の細胞種におけるA2ARの機能を厳密に制御することは、従来の薬理学的手法では困難でした。内因性リガンドへの応答性を維持しつつ、特定の阻害剤にのみ高感受性を示すA2AR変異体を設計できれば、細胞種特異的なA2ARのシグナル抑制が可能になると考えられますが、そのような変異体を設計・探索する手法は確立されていませんでした。
本研究では、A2ARをモデルとして、内因性リガンドであるアデノシンへの応答性を保持したまま、阻害剤ZM241385に高感受性を示すA2AR変異体の創出を目指しました。まず、無細胞タンパク質合成系に膜タンパク質を安定化するためのディスク状人工脂質膜(ナノディスク)を組み合わせることでA2ARを可溶発現し、ZM241385と特異的に結合することを確認しました。これにより、リボソームディスプレイ法[参考文献1]を用いた阻害剤結合能に基づくin vitro進化分子工学が可能となりました。次に、アデノシンおよびZM241385が結合したA2ARの構造情報を基に、飽和変異[用語6]を導入する2残基を選定しました。これらを全アミノ酸に置換した400種類の変異体ライブラリーを構築し、阻害剤結合に基づくスクリーニングを3回実施しました。得られた遺伝子配列を次世代シーケンサー(NGS)で解析したところ、特定変異を有するA2ARが顕著に濃縮されていました(図1A)。
同定した変異体をヒト由来の培養細胞株に導入し機能評価を行ったところ、内因性リガンドであるアデノシンへの応答性は野生型と同程度に維持されていました。一方で、ZM241385に対する感受性は10倍以上向上していました(図1B)。この結果は、同定されたA2AR変異体が、細胞内においても設計通りの機能を発現することを示しています。さらに、分子動力学シミュレーションにより、ZM241385に対する応答が向上した構造的要因を探索しました(図1C)。その結果、導入変異は直接的な相互作用の変化ではなく、構造的再配置を介してA2ARとZM241385の結合様式を変化させていることが分かりました。
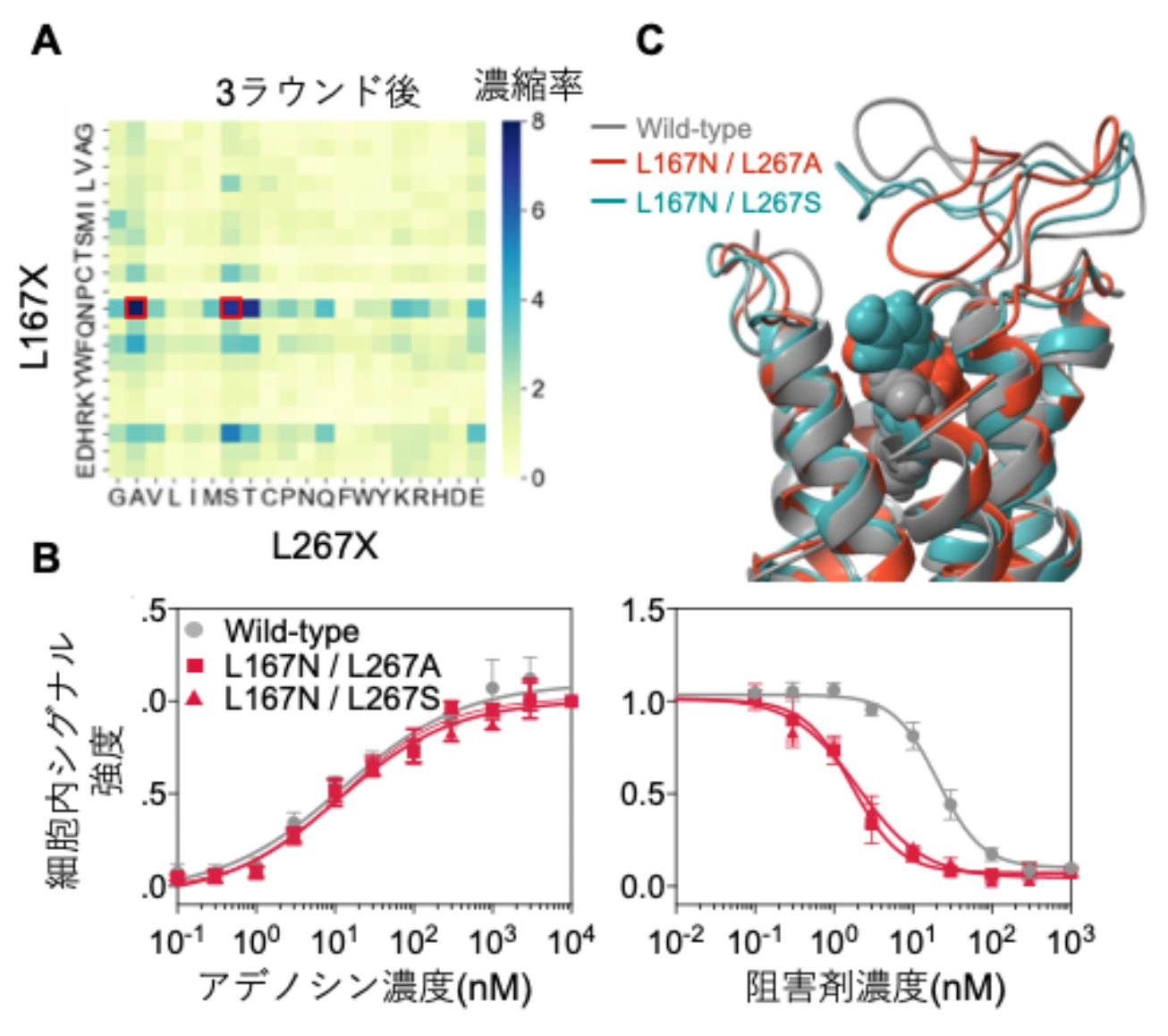
A) NGS解析の結果、400種類の変異体のうち赤で囲った2つが顕著に濃縮されていた。
B)取得した2つの変異体は、アデノシンでは野生型と同様に活性化されたが、阻害剤を加えた場合は、野生型よりも10倍低い阻害剤濃度で効果が見られた。
C)分子動力学シミュレーションの結果。野生型と変異体は阻害剤と異なる結合様式を持つことが分かった。
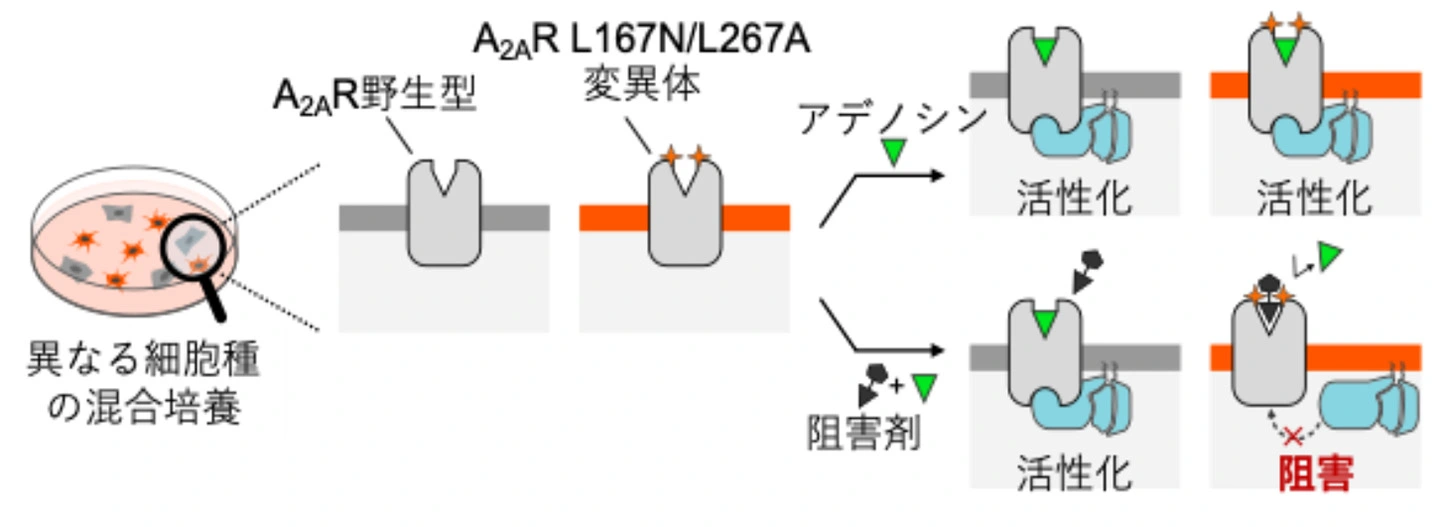
さらに本研究では、獲得した変異体の特性を応用し、異なる細胞種のうち特定細胞種のA2ARシグナルをZM241385により選択的に抑制できるかを検証しました。野生型または変異体を発現する細胞を共培養し、アデノシンとZM241385を添加したところ、変異体を発現する細胞群でのみA2ARシグナル抑制が起きていることを確認しました(図2)。この結果は、受容体分子設計と既存阻害剤の組み合わせにより、細胞種特異的なGPCRシグナル制御が可能であることを示唆しています。
社会的インパクト
本研究によって、細胞を用いることなく効率的に有用なGPCR変異体の取得が可能であることが示されました。この成果は、創薬研究への波及が期待されます。例えば、膜タンパク質の進化分子工学を加速し、GPCR創薬における受容体最適化やリガンド設計の新たな戦略を提供する可能性があります。また、本研究は既存の活性化型ケモジェネティクスに対して「阻害」に基づく制御戦略を提示するもので、技術の高度化にも寄与します。この制御戦略は、今後、生体内における受容体機能解析において高い汎用性を有すると考えられます。
今後の展開
本研究ではA2ARの2残基に飽和変異を導入し、限定的な配列空間(400種)から変異体をスクリーニングしました。しかし、in vitro進化分子工学では、ライブラリーサイズを1012規模まで拡張可能です。今後、より広範な配列領域に変異を導入することで、さらなる機能改変や新規特性の獲得が見込まれます。また、無細胞系では、温度や塩濃度などの条件を柔軟に制御できるため、細胞系では実施困難な条件下での人工進化実験も可能です。次世代シーケンサーから得られる大規模データと機械学習を組み合わせたライブラリー設計により、より効率的な変異体探索が実現すると考えられます。
将来的にはバイオセンシング、創薬、ケモジェネティクスなど幅広い分野への応用が期待されます。
付記
本研究は、ヒューマン・フロンティア・サイエンス・プログラム(HFSP)(RGP003/2023、RGEC29/2025)、JSPS科学研究費助成事業(22K21344、21H05228、24H00492、24KJ1275、23K14154、23H02445、24H01357、24H02259)、宮崎大学テニュアトラック推進室、AMED(JP24ama121013)、MEXT「富岳」成果創出加速プログラム(JPMXP1020230120)の支援を受けて実施されました。またMD計算は、TSUBAME4.0(東京科学大学)、スーパーコンピュータ富岳 (HPCI、理研、AMED(JP24ama121013))、岡崎計算科学研究センター(25-IMS-C045)、東京大学物性研究所 (2025-Ca-0038)で行われました。
参考文献
- [参考文献1]
- Porebski, B. T.; Balmforth, M.; Browne, G.; Riley, A.; Jamali, K.; Furst, M.; Velic, M.; Buchanan, A.; Minter, R.; Vaughan, T.; Holliger, P., Rapid discovery of high-affinity antibodies via massively parallel sequencing, ribosome display and affinity screening. Nat Biomed Eng 2024, 8 (3), 214-232.
- [参考文献2]
- Kondo, T.; Iwatani, Y.; Matsuoka, K.; Fujino, T.; Umemoto, S.; Yokomaku, Y.; Ishizaki, K.; Kito, S.; Sezaki, T.; Hayashi, G.; Murakami, H., Antibody-like proteins that capture and neutralize SARS-CoV-2. Sci Adv 2020, 6 (42), eabd3916.
- [参考文献3]
- Hanes, J.; Plückthun, A., In vitro selection and evolution of functional proteins by using ribosome display. Proc Natl Acad Sci U S A 1997, 94 (10), 4937-4942.
- [参考文献4]
- English, J. G.; Olsen, R. H. J.; Lansu, K.; Patel, M.; White, K.; Cockrell, A. S.; Singh, D.; Strachan, R. T.; Wacker, D.; Roth, B. L., VEGAS as a Platform for Facile Directed Evolution in Mammalian Cells. Cell 2019, 178 (3), 748-761 e17.
- [参考文献5]
- Klenk, C.; Scrivens, M.; Niederer, A.; Shi, S.; Mueller, L.; Gersz, E.; Zauderer, M.; Smith, E. S.; Strohner, R.; Plückthun, A., A Vaccinia-based system for directed evolution of GPCRs in mammalian cells. Nat Commun 2023, 14 (1), 1770.
- [参考文献6]
- Carpenter, B.; Lebon, G., Human Adenosine A(2A) Receptor: Molecular Mechanism of Ligand Binding and Activation. Front Pharmacol 2017, 8, 898.
用語説明
- [用語1]
- Gタンパク質共役型受容体(GPCR: G Protein-Coupled Receptor):細胞膜に存在する受容体タンパク質のファミリーで、ホルモンや神経伝達物質、光、匂い物質など、細胞外のシグナルを細胞内に伝える役割を担う。
- [用語2]
- 無細胞タンパク質合成系:転写に必要なRNAポリメラーゼや翻訳に必要なリボソームなどタンパク質合成に必要な成分を含む反応液である。試験管内で本反応液にDNA/mRNAを追加するだけでタンパク質を合成できる。
- [用語3]
- 次世代シーケンサー:DNAの塩基配列を高速かつ大量に読み取る技術。
- [用語4]
- ケモジェネティクス:遺伝子工学と化学物質を組み合わせて、特定の細胞内シグナル伝達を選択的に操作する技術。
- [用語5]
- リボソームディスプレイ法:mRNAとタンパク質を、リボソームを介して複合体を合成することで、標的タンパク質を提示するin vitro進化分子工学の手法。
- [用語6]
- 飽和変異:タンパク質の1つの残基を、天然で良く使われる20種類のアミノ酸に置換する変異の導入方法
論文情報
- 掲載誌:
- Journal of the American Chemical Society
- タイトル:
- In vitro evolution of the adenosine A2A receptor based on an antagonist binding using a ribosome display
- 著者:
- Genki Fukasawa#, Yuma Matsuoka#, Duy Phuoc Tran, Haruka Nishigaki, Keisuke Fukunaga, Takayoshi Watanabe, Tomohiro Doura, Naohiro Terasaka, Ako Kagawa, Takeshi Murata, Akio Kitao,* Shigeki Kiyonaka,* Tomoaki Matsuura*
( #: 共同筆頭著者、*: 責任著者) - DOI:
- 10.1021/jacs.6c02372
研究者プロフィール
深澤 元喜 Genki Fukasawa
東京科学大学 生命理工学院 生命理工学系 博士前期課程(研究当時)
研究分野:合成生物学
西垣 遥 Haruka Nishigaki
東京科学大学 生命理工学院 生命理工学系 博士前期課程2年
研究分野:合成生物学
福永 圭佑 Keisuke Fukunaga
東京科学大学 未来社会創成研究院 地球生命研究所 特任助教(研究当時)
宮崎大学 研究・産学地域連携推進機構 テニュアトラック推進室 准教授
研究分野:進化分子工学、核酸化学
チャン・フ・ズイ Duy Phuoc Tran
東京科学大学 生命理工学院 生命理工学系 助教
研究分野:理論物理学、計算生物物理学
北尾 彰朗 Akio Kitao
東京科学大学 生命理工学院 生命理工学系 教授
研究分野:生物物理学、計算生物学、計算化学
松浦 友亮 Tomoaki Matsuura
東京科学大学 未来社会創成研究院 地球生命研究所 教授
研究分野:生物工学、合成生物学、生物物理学
村田 武士 Takeshi Murata
千葉大学 大学院理学研究院 教授
研究分野:構造生物学、蛋白質工学
関連リンク
名古屋大学 総務部 広報課
千葉大学 企画部 渉外企画課 広報室
- koho-press@chiba-u.jp
- Tel
- 043-290-2232
- FAX
- 043-284-2550
宮崎大学 総務広報課
- Tel
- 0985-58-7114
- FAX
- 0985-58-2886