ポイント
- デュシェンヌ型筋ジストロフィー(DMD)は根本的な治療法が未確立の遺伝性筋疾患であり、アンチセンス核酸(ASO)を用いたエクソンスキッピング療法が一部の患者に適用されています。
- 現在の治療薬はPMOを用いたASOに限定されており、さらなる効果向上が求められています。
- 本研究では、DNAおよびLNAを基本骨格とするSSOに、核内送達を高める新技術「ヘテロ二本鎖核酸(HDSSO)」を初めて適用しました。
- HDSSOは従来型SSOに比べ高いエクソンスキッピング活性を示し、相補鎖構造と活性との関連も明らかにしました。
- この技術はLNAベース以外のSSOにも応用可能と考えられ、脂質やペプチドを用いた薬物送達技術との併用による標的指向性の向上も期待されます。
- 本成果は、スプライシング制御を目的とする幅広いアンチセンス核酸医薬の開発に貢献すると期待されます。
概要
核酸医薬は、従来の低分子化合物や抗体医薬では制御が困難なRNAを標的とすることが可能な、有望な医薬技術です。特にデュシェンヌ型筋ジストロフィーにおいては、スプライシングの制御を目的としアンチセンス核酸[用語1]医薬品が複数承認されています。一方で、これらのホスホロジアミデートモルホリノオリゴマー(PMO)[用語2]と呼ばれる核酸分子に限定されており、血中滞留性の短さや速やかな腎排泄といった薬物動態上の課題から、さらなる活性の向上が望まれています。
我々の研究室ではこれまでに、アンチセンス核酸の効果を大幅に向上させるヘテロ2本鎖核酸(HDO)技術を開発しており、PMOを用いたHDO技術も新たに開発しました。そして、デュシェンヌ型筋ジストロフィーの動物モデルであるmdxマウス[用語3]においても有効であることを報告しています。
今回、東京科学大学 脳神経病態学分野の横田隆徳名誉教授、長谷川樹里非常勤講師、核酸・ペプチド創薬治療研究センターの吉岡耕太郎特任講師らの研究グループは、大阪大学 大学院薬学研究科 生物有機化学分野の小比賀聡教授、下剛典大学院生(研究当時)らのグループとの共同研究により、HDO技術を応用し、モルフォリノ核酸(PMO)とは異なるDNAおよび糖鎖化学修飾(LNA)を基本骨格とするスプライススイッチングオリゴヌクレオチド(SSO:Splice-switching oligonucleotide)[用語4]の活性向上手法を検討しました。
まず、in vitroアッセイを用いて、多様な核酸化学修飾や鎖長のHDSSO分子を設計し、エクソンスキッピング活性への影響を評価した結果、エクソンスキッピング活性を向上させるHDSSO構造を同定しました。また、細胞内動態の解析から、HDO技術により核内への取り込みが増加し、相補鎖核酸の安定性の違いが核内移行効率に影響を与えることが明らかになりました。
さらに、デュシェンヌ型筋ジストロフィーのモデルマウスを用いたin vivo実験においても、HDO技術により高いエクソンスキッピング活性が示されました。
本研究は、HDO技術の応用によりLNAベースのSSOの活性を向上させうることを示したものであり、その成果は、国際科学誌「Molecular Therapy - Nucleic Acids」において、2025年3月11日にオンライン版で発表されました。
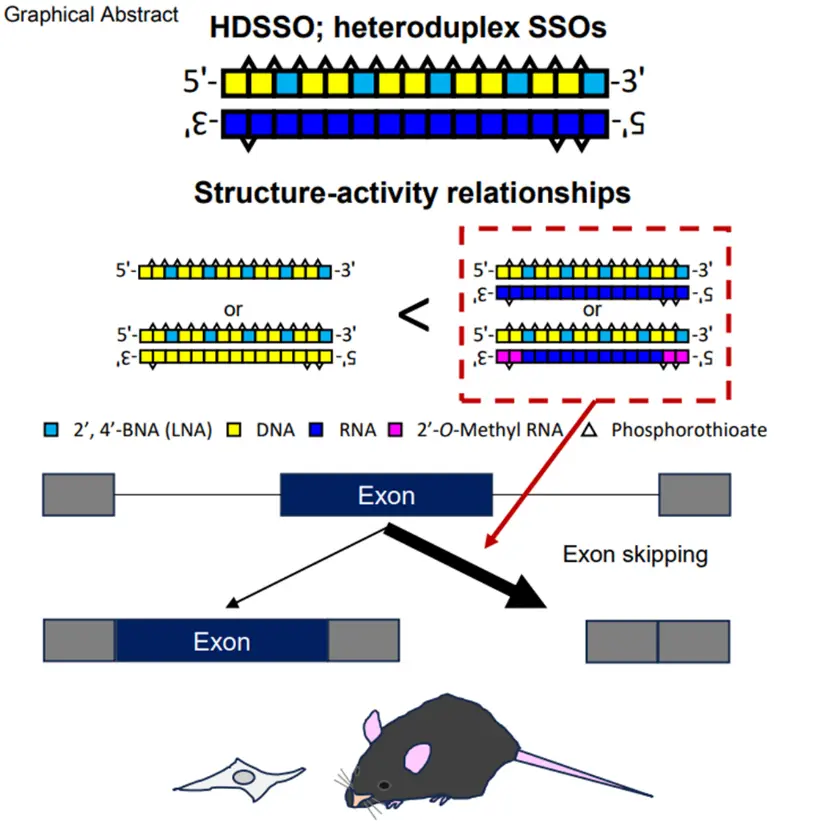
背景
核酸医薬を用いたプレ-mRNAのスプライシングの調節は、デュシェンヌ型筋ジストロフィー(DMD)や脊髄性筋萎縮症(SMA)を含む多くの遺伝性疾患に対する有望な治療戦略であり、まれな突然変異や遺伝性疾患に対する個別化治療である「n-of-1療法」にも応用が可能です。具体的には、スプライススイッチングオリゴヌクレオチド(SSO)と呼ばれるアンチセンス核酸医薬は、プレ-mRNAの標的領域に結合し、スプライシング因子の結合を阻害することで、mRNAの編集を通じてタンパク質発現を調節します。
デュシェンヌ型筋ジストロフィー(DMD)は、X染色体劣性遺伝の疾患であり、ジストロフィン遺伝子の異常によってジストロフィン蛋白質が産生されず、筋肉の変性や壊死が徐々に進行する難治性の病気です。近年では、異常のあるジストロフィン遺伝子内のエクソンを「読み飛ばす(エクソンスキッピング)」ことで、短縮型ながらも機能を有するジストロフィン蛋白を産生させるエクソンスキッピング療法[用語5]が、一部の遺伝子変異を有するDMD患者に対して実施されるようになりました。
この療法に用いられるのが、アンチセンス核酸(ASO)の一種であるSSOです。日本国内でも複数のSSOが承認されていますが、さらなる効果の向上が求められています。加えて、近年の研究では、ペプチドや低分子との結合などを通じたSSOの標的組織・細胞への送達効率の向上が注目されています。
そこで我々は、独自に開発した新規核酸医薬技術であるヘテロ二本鎖核酸(HDO)技術の、核内への高い送達性に着目し、このHDO技術を応用したSSO(HDSSO)の開発を進めることにしました。一方で、PMOや2’OMe RNAと相補鎖を組み合わせたHDSSOの報告はあるものの、糖鎖化学核酸(LNA)を基本骨格とするSSOへのHDO技術の応用は未報告であり、その構造設計と活性との関係も明らかではありませんでした。
そこで本研究では、エクソンスキッピング効率を高めるために必要な核内への効率的送達を実現することを目的として、DNAおよび糖鎖化学修飾(LNA)を基本骨格とする核酸を用いたHDSSOの開発に取り組みました。具体的には、まずin vitroアッセイにより相補的オリゴヌクレオチドの最適化を行い、その後、最適化したHDSSOをDMDモデルマウスであるmdxマウスに投与し、その治療効果を検討しました。
研究成果
まず、HDSSO技術がLNAベースのSSOおよび2’-OMe RNAベースのSSOに応用可能かを検討しました。ジストロフィン遺伝子を標的とした各SSOに対して、相補鎖としてDNA、RNA、または2'-OMe RNAホスホロチオエート修飾(Wing)を含む3種類を設計し(図1A)、1本鎖SSO(Single)とHDSSOのエクソンスキッピング活性をin vitroで比較しました。
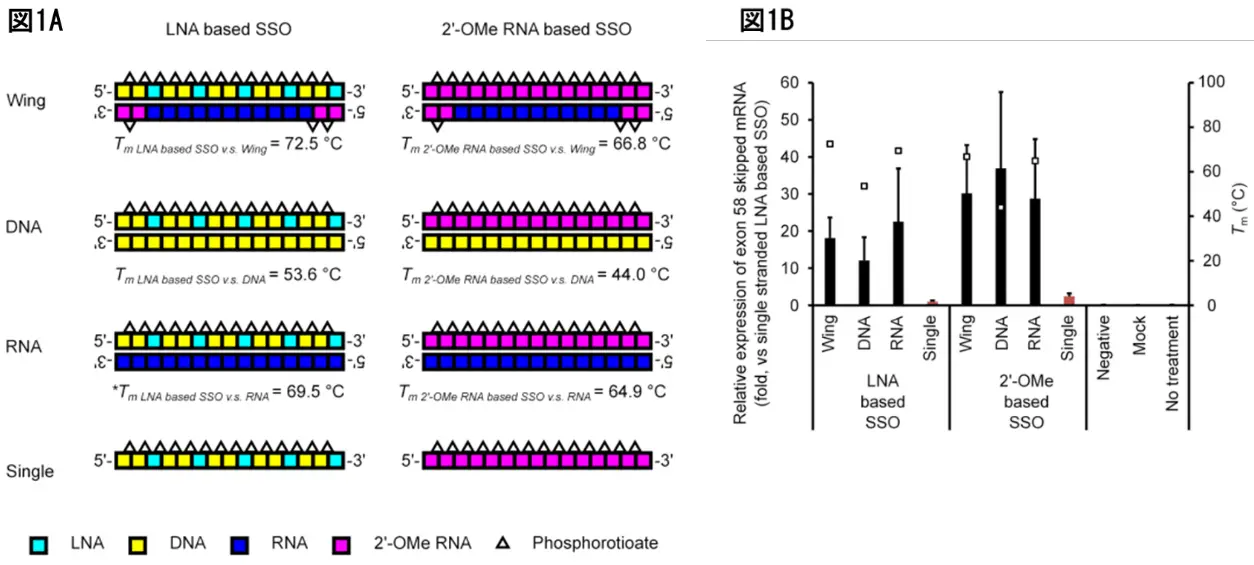
その結果、HDSSOはいずれのベースでもSingleよりも高い活性を示しました(図1B)。また、相補鎖の融解温度(Tm)測定では、DNA鎖の結合安定性が最も低い結果となりました。
次に、相補鎖の構造がHDSSOの活性に与える影響を評価しました。
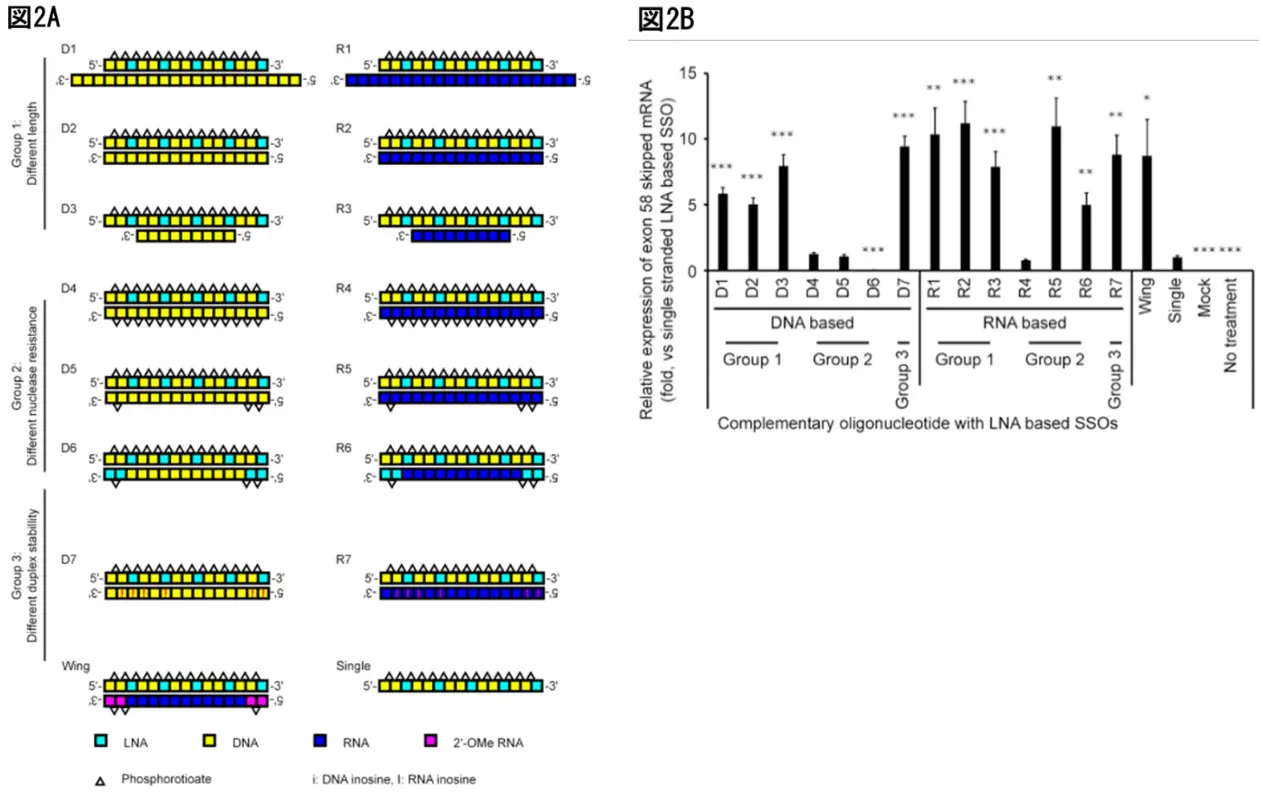
グループ1では、長さの異なるDNA、またはRNA相補鎖(9〜21 mer)を用いたHDSSOを比較し、DNAベースでは9 mer(D3)が最も高い活性を示しました(図2A、2B)。RNAベースでは明確な差はありませんでした。
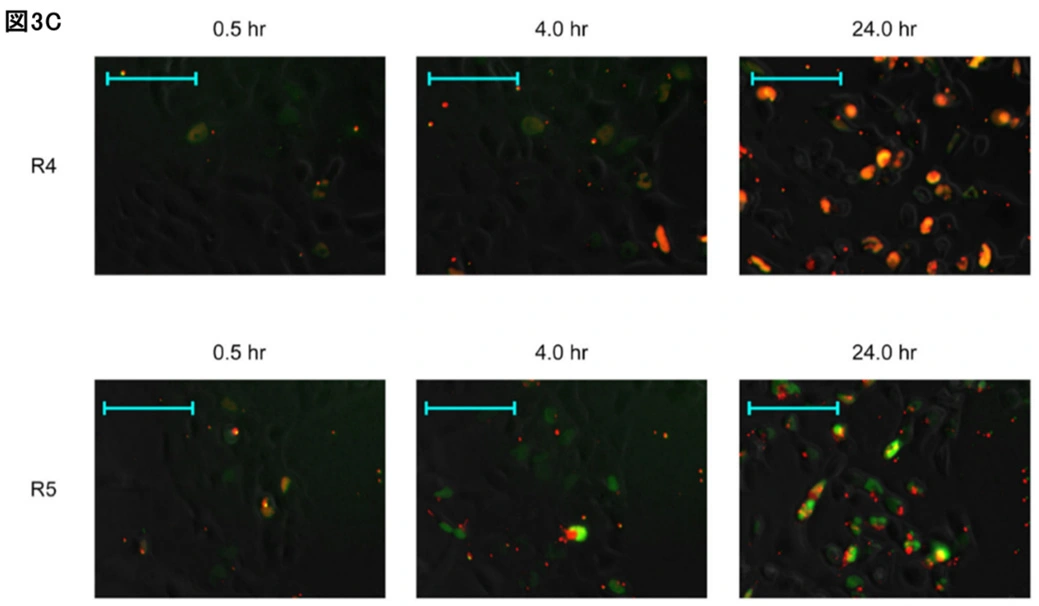
グループ2では、PS結合やLNA修飾の有無を変えた相補鎖を設計し、活性を評価しました。全PS修飾のR4やD4は低活性でしたが、5’/3’末端のみPS修飾のR5は高い活性を維持し、LNAを加えたR6は中程度の活性を示しました(図2B)。
グループ3では、相補鎖中のグアニンをイノシンに置換(G>I)したD7/R7を設計しました。G>I置換により、HDSSOの結合親和性(Tm値)が低下すると考えましたが、DNAベースHDSSOでは活性が上昇しましたが、RNAベースでは有意な変化は見られませんでした。
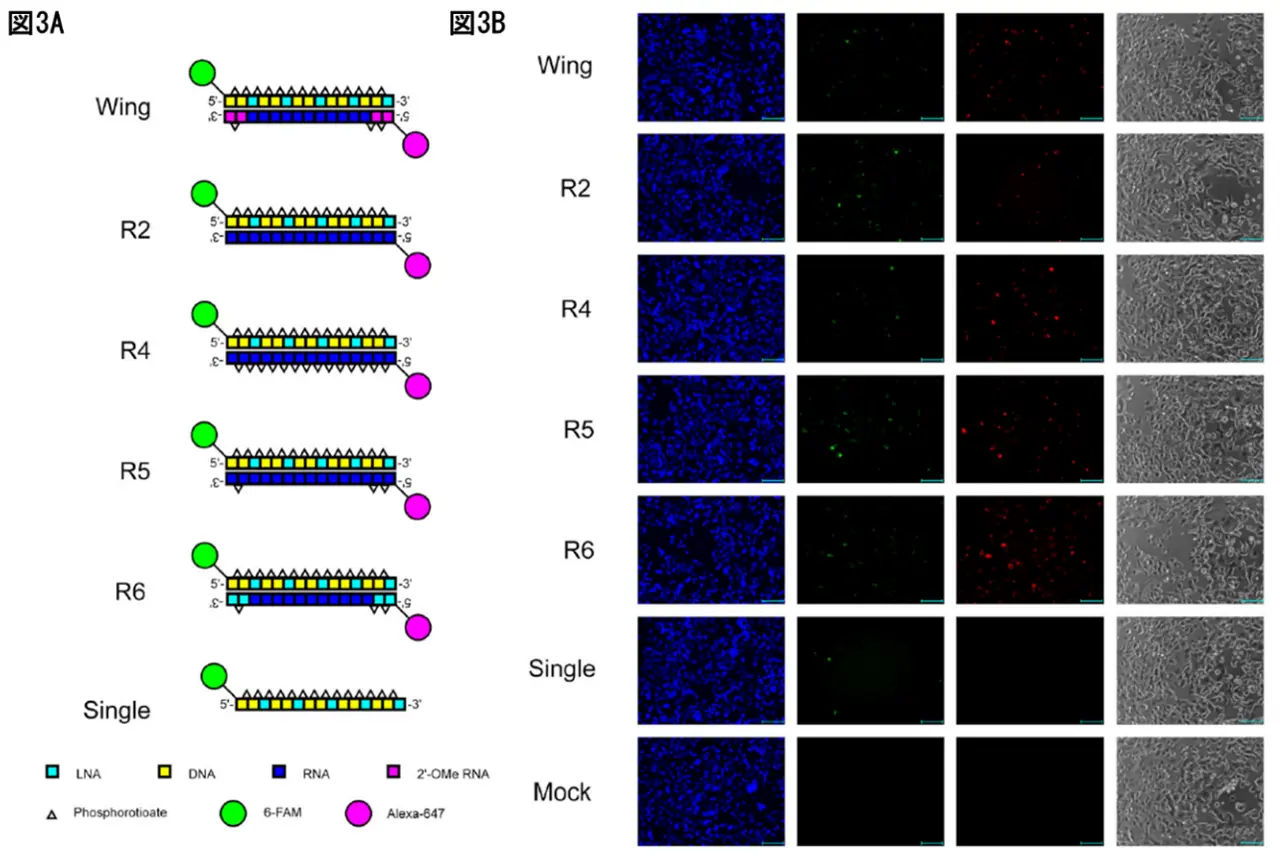
次に、細胞内でのHDSSO挙動を評価するため、グループ2の相補鎖R4〜R6とコントロールとしてwing、R2、Singleを用いて、SSOおよび相補鎖を蛍光標識してタイムラプス観察を行いました(図3A、3B)。導入30分後には全てのHDSSOで核内に両蛍光が確認されました。活性の高いR2やR5を含むHDSSOでは、時間経過とともに赤色蛍光(相補鎖由来)が減少し、相補鎖が核内から消失したと推測されました。一方、R4を含むHDSSOでは赤色蛍光が長時間残存し、相補鎖の排出・分解の遅れが活性低下の一因と考えられました(図3C)。
最後に、R5設計に基づいたHDSSOを用いたin vivo評価を行いました。mdxマウスの変異に合わせてSSO配列を再設計し、R5相補鎖のHDSSOおよび全PS結合のHDSSO(full PS)を投与しました(図4A)。筋注後、HDSSOはfull PSより高いエクソンスキッピング活性を示し、Singleよりも効果的でした(図4B)。IHC解析ではHDSSOのジストロフィン蛋白質の発現増加が確認され(図4C)、ウエスタンブロッティングでもHDSSOがSingleより高い発現を示しました(図4D)。
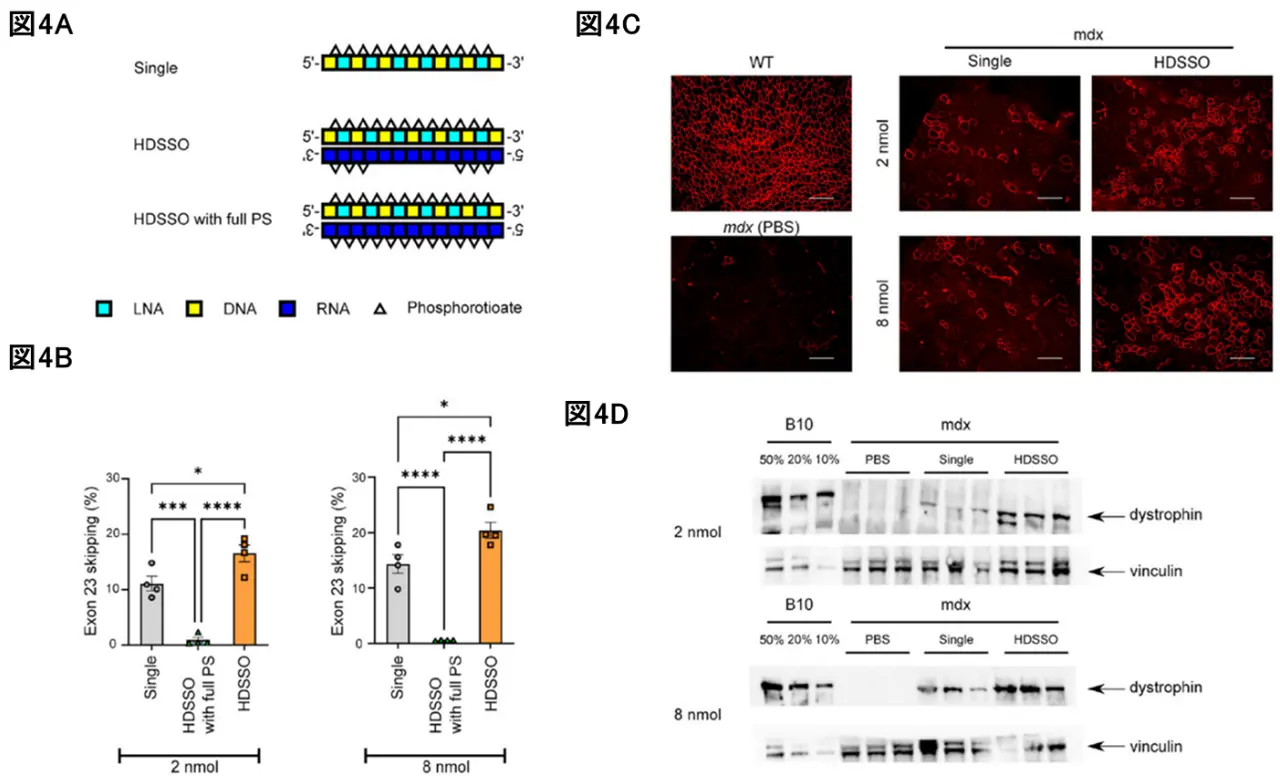
本研究により、HDSSOの活性は相補鎖の種類、長さ、修飾に大きく依存すること、また細胞内での相補鎖の挙動が活性に影響することが明らかとなりました。さらに、in vivoにおいてもHDSSOの優れたエクソンスキッピング効果が確認されました。
今後の展開
デュシェンヌ型筋ジストロフィーは、依然として有効な治療法が確立されていない遺伝性疾患であり、新たな核酸医薬の開発が期待されています。本研究では、核内送達を効率化するヘテロ2本鎖核酸(HDO)技術をDNAおよびLNAベースのSSOに初めて応用し、優れたエクソンスキッピング活性を示すHDSSO構造を同定しました。また、相補鎖の構造と活性の関係性も明らかにし、細胞内で高い活性を示す設計指針を得ることができました。
このHDSSO技術は、LNAベースのSSOに限らず、他の核酸修飾にも応用可能と考えられます。さらに、現在注目されている脂質やペプチドを用いた薬物送達技術と併用することで、標的臓器への送達性の向上も期待されます。
以上より、本技術は筋組織に限らず、多様な標的組織におけるスプライシング制御型治療法の基盤となりうるものであり、アンチセンス核酸医薬の幅広い応用に貢献すると期待されます。
用語説明
- [用語1]
- アンチセンス核酸(ASO):核酸医薬の1種であり、標的の遺伝子のRNAなどに作用する。具体的にはASOは天然の核酸及び様々な化学修飾が施された1本鎖の核酸構造を基本構造として、標的のRNA等と結合し、標的RNAを分解、または立体障害をきたすことで、RNAの制御を行う。
- [用語2]
- ホスホロジアミデートモルホリノオリゴマー (PMO):核酸は生体内でヌクレアーゼにより分解されやすく、化学修飾を施した核酸医薬が開発されているが、細胞毒性も問題となっている。PMOは核酸類似の人工化合物であるモルフォリン環を持ち、ホスホロジアミデート結合をしていることでヌクレアーゼ耐性が高く細胞毒性が低い利点があるが、電荷をもたないため、細胞膜透過性が低く組織移行性が低いことが課題である。
- [用語3]
- mdxマウス:X染色体上にあるジストロフィン遺伝子のエクソン23に点突然変異を持っており、ジストロフィン蛋白が作られないため、デュシェンヌ型筋ジストロフィーのモデルマウスとなっている。
- [用語4]
- スプライススイッチングオリゴヌクレオチド(SSO:Splice-switching oligonucleotide):アンチセンス核酸(ASO)の作用機序のうち、プレ-mRNAの標的領域に結合し、プレ-mRNAのスプライシング因子の結合を阻害することで、mRNAを調整し、その後の蛋白発現を調整する。
- [用語5]
- エクソンスキッピング療法:成熟したmRNAになる前の未熟なRNAに作用して、異常なエクソンを翻訳させないようにして(エクソンスキッピング)、正常よりも少し短いながら正常に機能する標的蛋白質を作らせる治療法である。
論文情報
- 掲載誌:
- Molecular Therapy - Nucleic Acids
- タイトル:
- Effect of chemical modification on the exon skipping activity of heteroduplex oligonucleotides
- 著者:
- Takenori Shimo, Juri Hasegawa(共著者), Kotaro Yoshioka, Yusuke Nakatsuji, Kotomi Aso, Keisuke Tachibana, Tetsuya Nagata, Takanori Yokota, and Satoshi Obika
研究者プロフィール
長谷川 樹里 Juri Hasegawa
東京科学大学 大学院医歯学総合研究科
脳神経病態学分野(脳神経内科) 非常勤講師
研究領域:神経内科学、核酸医薬

吉岡 耕太郎 Kotaro Yoshioka
東京科学大学 総合研究院
核酸・ペプチド創薬治療研究センター(TIDEセンター) 特任講師
脳神経病態学分野兼担
研究領域:神経内科学、核酸医薬

横田 隆徳 Takanori Yokota
東京科学大学 大学院医歯学総合研究科
脳神経病態学分野(脳神経内科) 名誉教授
研究領域:神経内科学、核酸医

小比賀 聡 Satoshi Obika
大阪大学 大学院薬学研究科
生物有機化学分野 教授
研究領域:生物有機化学、核酸化学

下 剛典 Takenori Shimo
大阪大学 大学院薬学研究科 生物有機化学分野 大学院生(研究当時)
研究領域:生物有機化学、核酸化学
関連リンク
お問い合わせ
東京科学大学 大学院医歯学総合研究科 脳神経病態学分野
特任講師 吉岡 耕太郎
- kotanuro@tmd.ac.jp
- Tel
- 03-5803-5234
- Fax
- 03-5803-0169