創薬標的受容体の活性化を制御するトリプトファンに富む「アロステリック・ネットワーク」を解明
数理アロステリー解析、NMR、分子シミュレーションを統合し、長距離情報伝達経路を明らかに
ポイント
- 代表的なGタンパク質共役型受容体(GPCR)で、重要な創薬標的である「ヒトA2Aアデノシン受容体(A2AR)」の活性化を保存的なナトリウム結合ポケットとトリプトファン残基が協調して制御する機構である「アロステリック・ネットワーク」を解明
- 19F NMR、剛性理論に基づくアロステリー解析(RTA)、および分子シミュレーションを組み合わせることで、長距離情報伝達経路とどのように結びつくかを解明
- GPCR活性化とアロステリーの理解を深め、将来的なアロステリックGPCR創薬の発展への貢献を期待
概要
東京科学大学 生命理工学院のTran Phuoc Duy(チャン・フ・ズイ)助教と北尾彰朗教授、理化学研究所のアドナン・スリオカ研究員、トロント大学のスコット・プロッサー教授らを中心とする国際共同研究チームは、主要なGタンパク質共役型受容体(GPCR)で、創薬標的でもある「ヒトA2Aアデノシン受容体(A2AR)」の活性化が、タンパク質を構成するアミノ酸の1つであるトリプトファンに富む「アロステリック・ネットワーク[用語1]」によって、どのように促進するかを明らかにしました。
研究チームは、機能アッセイ、フッ素19核磁気共鳴(19F-NMR)、剛性理論に基づくアロステリーの数理モデリング、ならびに分子シミュレーションを組み合わせることで、主要なトリプトファン残基における局所的な構造変化が、リガンド結合ポケットから細胞内のGタンパク質カップリング機構へと至る長距離の情報伝達経路と結びついていることを明らかにしました。具体的には、主要なアロステリック・ネットワークの内部に、トリプトファンに富むネットワークが埋め込まれていることを同定し、このことがGPCR活性化におけるアロステリック情報伝達に機能的に関与しうることを明らかにしました。
本研究はまた、受容体に保存的に存在するナトリウム結合ポケットの機能的役割も明確にしました。具体的には、ナトリウムの放出[用語2]によりGPCRの活性化に関連する構造状態変化が強く促進されること、さらにGタンパク質と相互作用する準備段階と考えられるプレカップル状態を増強することも示しました。
これらの成果は、GPCR活性化とアロステリーの理解を深め、将来的なアロステリックGPCR創薬の発展に貢献する可能性が期待されます。
本成果は、3月2日付(米国東部時間 午後3時)の「Proceedings of National Academy of Science, U.S.A.」誌に掲載されました。
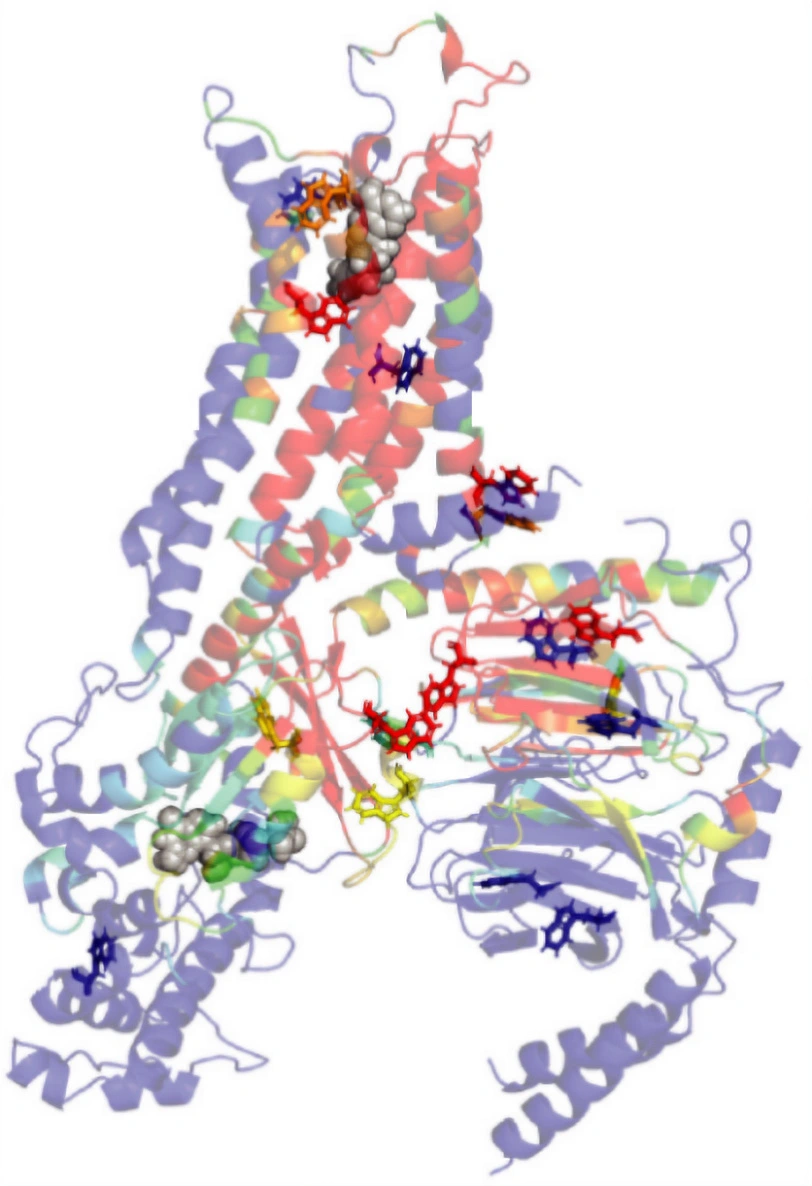
剛性理論に基づく計算解析は、アデノシンA2A受容体(A2AR)の活性化が、長距離アロステリック情報伝達経路(赤および他の明るい色でハイライト)によって制御されることを示している。多数のトリプトファン残基(スティック表示)がこれらの経路上に位置しており、GPCRの活性化と機能状態の制御に関わるアロステリック・ネットワークの重要な結節点(ノード)として機能することを支持する。
背景
Gタンパク質共役型受容体(GPCR)は、ヒトにおける膜受容体ファミリーの中で最大であり、現代医療における重要な創薬標的の1つです。多くの承認薬がGPCRを標的としている一方で、強力かつ高選択的な治療薬の設計は依然として難しい状況です。これはGPCRの機能が静的な構造だけでは決まらず、受容体内および受容体とシグナル伝達パートナー間に存在する長距離アロステリック情報伝達によって制御される動的なコンフォメーション変化に依存するためです。
本研究では、代表的なクラスA GPCRである「A2Aアデノシン受容体(A2AR)[用語3]」に着目しました。A2ARは主要なGSシグナル伝達に加え、他のGタンパク質とも相互作用し得ることが報告されており、GPCRシグナルにおけるGタンパク質選択性と有効を理解するという広範な課題を象徴する系で、様々な薬の標的となっています。薬理作用は、アゴニスト(作動薬)/アンタゴニスト(拮抗薬)という枠組みで理解されがちですが、GPCRがアロステリック経路を通じて選択性、有効性、バイアス型シグナル伝達をどのように制御するかについて、より深い機構理解が得られれば、次世代の薬理学に新たな可能性が開かれます。
これまでの構造・生化学研究により、重要なマイクロスイッチと呼ばれるアミノ酸残基やそのネットワーク、クラスA GPCRに保存的なナトリウム結合ポケットの存在が示されてきました。しかし、これら局所要素が受容体–Gタンパク質複合体全体の活性化やカップリングにどのように結びつくかには、多くの不明点があります。
研究成果
本研究では、理化学研究所のアドナン・スリオカ研究員が発明・開発した剛性理論に基づくアロステリー解析(RTA)と19F-NMRと分子シミュレーションを統合し、A2ARおよび受容体–Gタンパク質複合体における情報伝達経路を直接追跡しました。19F-NMR実験はプロッサー教授(トロント大学)が主導し、分子動力学(MD)シミュレーションはTran 助教と北尾教授(東京科学大学)、モンテカルロ(MC)シミュレーションはAndrejs Tucs研究員(理化学研究所)が実施しました。
1. 数理アロステリー解析、19F-NMR、分子シミュレーションの統合
本研究は、RTAから開始し、アゴニストが結合したA2AR–Gタンパク質複合体における顕著なアロステリック情報伝達経路を予測するとともに、その経路上に多数のトリプトファン残基が関与することを示しました。次に研究チームは、19F-NMRによりこれら予測を実験的に検証しました。具体的には、全体的な活性化状態の変化を反映する膜貫通ヘリックス6と、A2ARに分布する複数のトリプトファン部位の局所構造変化を反映するフッ素化トリプトファンレポーターという2つの相補的な情報によって、受容体のコンフォメーション変化を追跡しました。
さらに、実験と機構を結びつけるため、MDシミュレーションと、剛性・幾何情報に基づくMCシミュレーションを用いて、立体構造分布を特徴づけ、特定の残基やマイクロスイッチが長距離カップリングにどのように寄与するかを解釈しました。MDシミュレーションは、主要マイクロスイッチ領域とナトリウム結合ポケットが活性化関連アンサンブル間でどのように再編成されるかを示し、NMRで観測された立体構造分布変化に対する構造的解釈を与えました。MCシミュレーションは、様々な立体構造を効率よく探索することで、これを補強し、不活性状態と活性化状態を結ぶ妥当な経路や中間状態を提示しました。
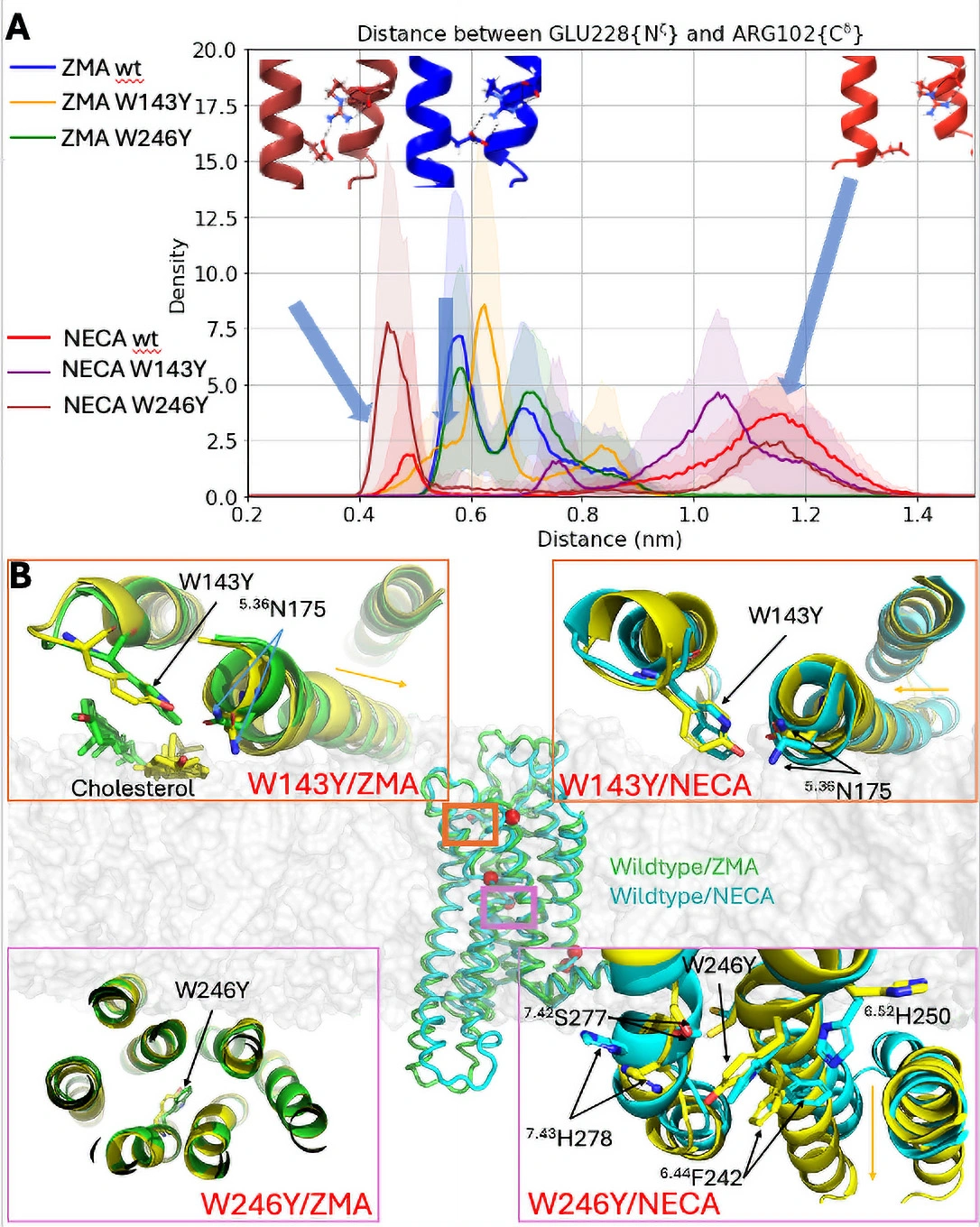
2. トリプトファンに富むアロステリック・ネットワークの発見
本研究の中心的な成果は、剛性理論により予測された主要なアロステリック情報伝達経路の内部に、トリプトファンに富むネットワークが埋め込まれていることを同定した点です。これは、トリプトファンが単なる受動的な構造要素や便利なNMRプローブにとどまらず、GPCR活性化におけるアロステリック情報伝達に機能的に関与することを示唆するものです。特に、進化的に保存されたトグルスイッチ残基W246および細胞外ループ残基W143の重要性が示されました。変異体(W246Y、W143Y)解析と19F-NMR、シミュレーションにより、これら部位の摂動が受容体の立体構造の挙動に長距離効果をもたらすことが明らかになり、アロステリック情報伝達制御における役割が支持されました。
3. ナトリウム放出が活性化関連状態を促進
もう一つの成果は、クラスA GPCRで保存されているナトリウム結合ポケットの機能的重要性に対する機構的説明ができたことです。高ナトリウム条件では不活性状態が安定化される一方、低ナトリウム条件では活性化関連の立体構造分布が強く促進されました。特にナトリウムの枯渇は、Gタンパク質との生産的カップリングに先行すると考えられるプレカップル状態を強く増強しています。
これらの結果は、保存的ポケットからのナトリウム放出がGPCR活性化を可能にする鍵となるステップであり、シグナル伝達に必要な活性型立体構造への移行を促進することを示しています。
社会的インパクト
ナトリウム結合ポケットおよび関連する活性化モチーフはクラスA GPCRに広く保存されているため、本成果はA2ARにとどまらず、多くの医学的に重要な受容体の活性化機構理解にも寄与すると期待されます。さらに本研究によって、イオン依存的制御、マイクロスイッチのダイナミクス、トリプトファン媒介のアロステリック情報伝達、受容体–Gタンパク質シグナル伝達を統合的に結びつける枠組みを提示したことは、今後のGPCR創薬の新たな可能性を広げるものとなり得ます。また本研究は、実験的生物物理と数理モデリング、先端シミュレーションを組み合わせることが、構造生物学と創薬における複雑で動的な問題の解決に有効であることを示しています。
今後の展開
本研究は、19F-NMR、剛性理論に基づくアロステリー解析(RTA)、および分子動力学シミュレーションに基づく構造解析を統合し、GPCRの活性化およびカップリング機構を研究するための強力な枠組みを確立しました。今後、このアプローチを、他のクラスA GPCRや他ファミリーGPCR、多様な受容体–Gタンパク質ペア、疾患関連変異体、バイアスドシグナリングを含むリガンド依存的活性化経路などへ展開することを検討しています。具体的には、受容体特異的なアロステリック経路や活性化中間体を同定することで、選択性が高く副作用の少ない次世代GPCR治療薬やアロステリックモジュレーターの合理的設計につなげていきたいと考えています。
付記
本研究は、科学研究費助成事業(課題番号:JP23H04058、JP24H02259、JP24H01357)の支援を受けて行われました。
本研究の計算においては、北尾研究室のPCクラスターの使用に加え、東京科学大学TSUBAME4.0、東京大学物性研究所のスーパーコンピュータ(課題番号: 2025-Ca-0038)、自然科学研究機構計算科学研究センターのスーパーコンピュータ(課題番号: 25-IMS-C046)、理化学研究所のスーパーコンピュータ「富岳」(課題番号:hp240221、hp250220)の計算資源の提供を受けました。
用語説明
- [用語1]
- アロステリック・ネットワーク:タンパク質へのある分子の結合が、結合部位から離れたタンパク質の別の部位と相互に影響を及ぼし合う仕組み(ネットワーク)のこと。アロステリーはその効果のこと。
- [用語2]
- ナトリウムの放出:多くのGタンパク質共役型受容体(GPCR)には、受容体内部にナトリウムイオン(Na+)が結合する保存的なポケットが存在する。ここではナトリウム濃度が低い状態で、このポケットからナトリウムイオンが離れる現象を「ナトリウムの放出」と呼び、受容体の活性化やGタンパク質との結合に関与すると考えられている。
- [用語3]
- A2Aアデノシン受容体(A2AR):神経系、血小板、免疫細胞、肺、心臓、血管系に広く分布するGタンパク質共役型受容体(GPCR)で、創傷、血管疾患(動脈硬化、再狭窄、血小板活性化など)、炎症やがんなどの多様な薬剤の標的となっている。
論文情報
- 掲載誌:
- Proceedings of National Academy of Science, U.S.A.
- タイトル:
- The Role of the Tryptophan-Rich Allosteric Network and Sodium Egress in GPCR Activation
- 著者:
- Zhenzhou Qi , Duy Phuoc Tran , Andrejs Tucs , Roopan Thiara , Louis-Philippe Picard , Koji Tsuda , Aditya Pandey , Adnan Sljoka , Akio Kitao , Robert Scott Prosser
研究者プロフィール
チャン・フ・ズイ Duy Phuoc Tran
東京科学大学 生命理工学院 生命理工学系 助教
研究分野:理論物理学、計算生物物理学
北尾 彰朗 Akio Kitao
東京科学大学 生命理工学院 生命理工学系 教授
研究分野:生物物理学、計算化学、計算生物学
アドナン・スリオカ Adnan Sljoka
理化学研究所 革新知能統合研究センター 研究員
研究分野:数理モデリング