ポイント
- タンパク質との重要な分子間相互作用を維持したまま新規分子を生成するAIを開発
- 拡散モデルを用いてタンパク質の結合ポケット内で直接3次元分子を設計
- SARS-CoV-2メインプロテアーゼを対象に有望な薬候補分子の設計可能性を確認
概要
東京科学大学(Science Tokyo) 情報理工学院 情報工学系の関嶋政和准教授らの研究グループは、タンパク質と薬候補分子の相互作用を制約条件として取り入れた分子生成AI「DiffPharma」を開発しました。
薬は、標的タンパク質に結合してその働きを制御することで効果を発揮します。この関係はしばしば「鍵と鍵穴モデル」で説明され、タンパク質の結合ポケット[用語1]に対して薬分子(鍵)が正しく適合する必要があります。しかし実際の結合は単なる形状の一致だけではなく、水素結合や疎水相互作用などの複数の分子間相互作用[用語2]が組み合わさることで安定化しています。
今回開発したDiffPharmaは拡散モデル[用語3]を用いており、分子間相互作用をAIの分子生成過程に組み込み、タンパク質との結合様式を保ったまま新しい分子を設計できる技術です。評価実験では、生成された分子が既知の活性分子と同様の相互作用パターンを高い精度で再現し、既存の分子生成AIを上回る性能を示しました。さらに、SARS-CoV-2メインプロテアーゼを対象とした解析では、既知阻害剤と同等あるいはそれ以上の結合傾向を示す候補分子が得られました。本研究は、AIを活用した創薬研究において、タンパク質との相互作用を考慮した分子設計を可能にする新しいアプローチを示すものです。
本成果は、2026年3月2日付(現地時間)の「npj Drug Discovery 」誌に掲載されました 。
背景
新薬開発において、標的タンパク質の立体構造を基に薬候補分子を設計する、構造ベース創薬[用語4]が広く用いられています。
薬分子はタンパク質の結合ポケットに入り込み、タンパク質の働きを阻害・調節することで薬効を発揮します。この関係は「鍵と鍵穴モデル」で説明されるように、分子の形状がタンパク質に適合することが重要です(図1)。
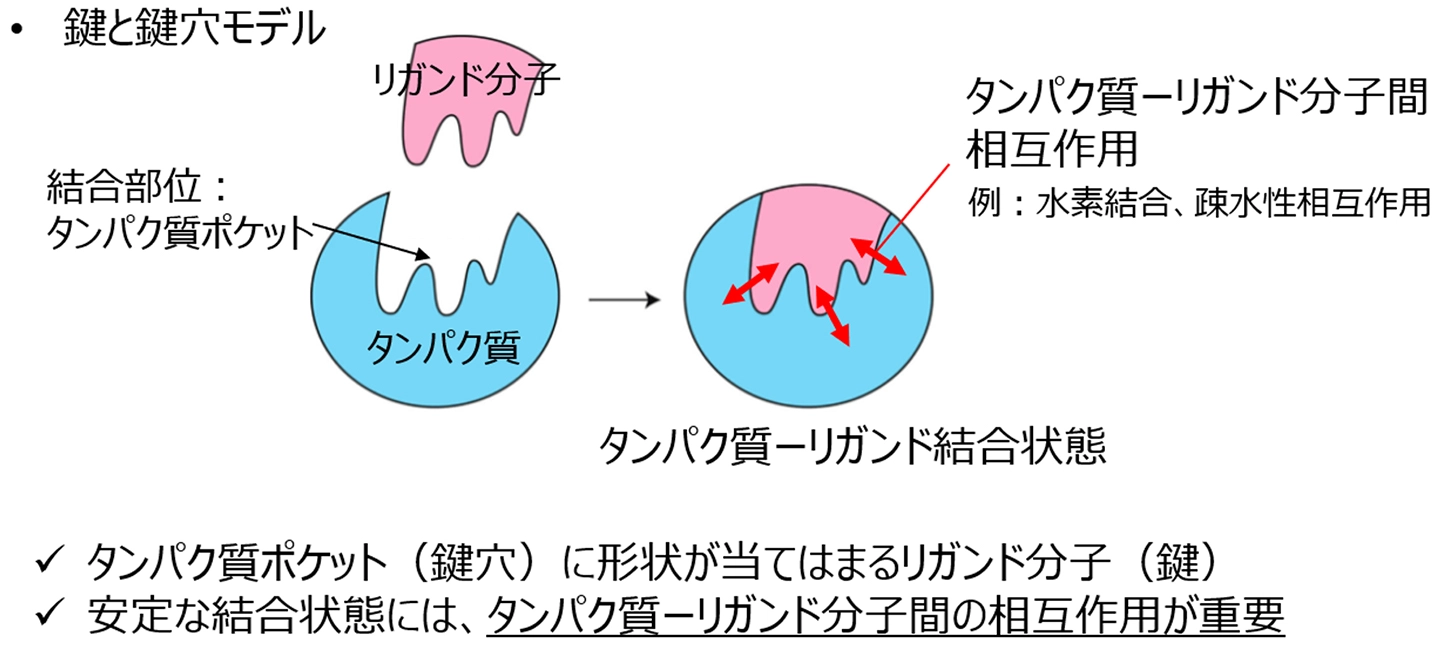
しかし実際の分子認識では、形状だけでなく水素結合、疎水性相互作用、π–π相互作用などの複数の分子間相互作用が正しく配置されることが、薬の効果を決定づけます。一方、薬として利用可能な分子の候補数は1060以上と推定されるほど膨大であり、既存の化合物データベースからの探索ではその一部しか調べることができません。近年、AIを用いて新しい分子構造を設計する研究が進んでいますが、多くの手法ではタンパク質との相互作用を十分に再現できず、結合様式を維持した分子設計が難しいという課題がありました。
研究成果
研究チームは、タンパク質と薬候補分子の相互作用を明示的に取り入れた分子生成AI「DiffPharma」を開発しました。この手法では、水素結合や疎水性相互作用などの分子間相互作用を「相互作用粒子」として空間上に配置し、それらを手掛かりとして拡散モデルによって分子構造を生成します。これにより、タンパク質の結合ポケットに対して
- 形状が適合する
- 必要な相互作用が形成される
という条件を同時に満たす分子を三次元構造として設計することが可能になりました。さらに、タンパク質―分子関係、水素結合、疎水相互作用をそれぞれ学習する複数のニューラルネットワークを統合する新しいAIアーキテクチャを導入し、複数の相互作用を同時に満たす分子生成を実現しました。
100種類のタンパク質―リガンド複合体を用いた評価では、生成された分子は参照分子と非常に類似した相互作用パターンを示し、残基レベルで最大0.9の相互作用類似度を達成しました。これは既存の分子生成手法の0.6を大きく上回る結果です。
また、AKTキナーゼやβラクタマーゼなどの創薬ターゲットタンパク質に対して新規分子を生成した結果、重要な相互作用を維持したまま異なる化学構造を持つ分子系列を設計できることが確認されました(図2)。特に図2に示すように、生成された分子は既知分子とほぼ同様の相互作用パターン(点線の結ばれ方)を維持しており、結合様式を保ったまま構造の異なる分子を複数設計できていることが分かります。
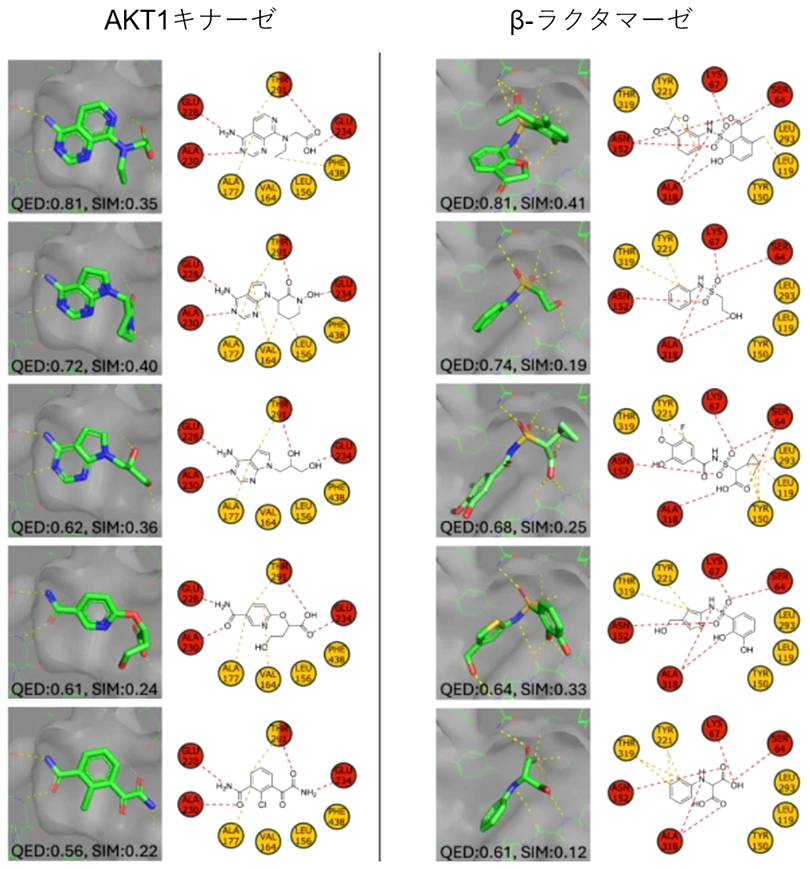
本研究で開発したAIは、タンパク質の結合ポケットに適合するだけでなく、水素結合や疎水相互作用などの重要な分子間相互作用を維持したまま新規分子を生成する。各例では、生成分子(左)と対応する相互作用パターン(右)を示しており、既知分子とは異なる構造でありながら、同様の結合様式が再現されている。黄色や赤色の丸は、タンパク質中の相互作用に関与するアミノ酸残基を示し、黄色線は水素結合、赤線は疎水性相互作用を表している。
さらに、新型コロナウイルス感染症(COVID-19)の原因ウイルスであるSARS-CoV 2のメインプロテアーゼを対象とした解析では、分子動力学シミュレーション[用語5]および結合自由エネルギー計算により、既知阻害剤と同等あるいはそれ以上の結合傾向を示す候補分子が得られました。
社会的インパクト
本研究は、タンパク質との結合様式を保ったまま新しい分子を設計できるAI技術を実現したものであり、従来の創薬プロセスにおける候補分子探索の効率を大きく向上させる可能性があります。これにより、新薬開発に要する時間やコストの削減につながるだけでなく、これまで探索が困難であった新規化学空間からの薬候補分子の発見が期待されます。また、本手法は幅広い疾患領域に応用可能であり、AI創薬の実用化を加速し、人々の健康と医療の発展に貢献することが期待されます。
今後の展開
今回開発したDiffPharmaは、タンパク質との相互作用を維持した分子設計を可能にする新しい創薬AIです。今後は、π–π相互作用など他の分子間相互作用の導入や、薬物動態や物性を同時に最適化するAI技術と組み合わせることで、創薬研究を大きく加速させる技術としての応用を進めます。
付記
今回の研究成果は、以下の事業の支援を受けて実施されました。
- 日本医療研究開発機構(AMED)生命科学・創薬研究支援基盤事業(BINDS)(JP25ama121026)
- 日本学術振興会(JSPS)科学研究費助成事業 学術変革領域研究(A)「天然物が織り成す化合物潜在空間が拓く生物活性分子デザイン」(JP24H01760)
用語説明
- [用語1]
- 結合ポケット:タンパク質の表面に存在するくぼみ状の領域で、薬分子などの小分子が結合する場所。薬はこのポケットに結合することでタンパク質の働きを阻害または調節する。
- [用語2]
- 分子間相互作用:分子同士が引き合う力の総称。水素結合、疎水相互作用、π–π相互作用などがあり、薬分子がタンパク質に安定して結合するために重要な役割を果たす。
- [用語3]
- 拡散モデル:ノイズから徐々に情報を復元してデータを生成するAIモデル。画像生成AIなどでも使われており、本研究ではタンパク質の結合ポケットに適合する薬候補分子の三次元構造を生成するために用いられている。
- [用語4]
- 構造ベース創薬:タンパク質の三次元構造をもとに薬候補分子を設計する創薬手法。X線結晶構造解析や計算機シミュレーションなどを用いて、タンパク質の結合ポケットに適合する分子を設計する。
- [用語5]
- 分子動力学シミュレーション:分子の動きをコンピュータ上で再現する計算手法。タンパク質と薬分子がどのように結合し、時間とともにどのように振る舞うかを原子レベルで解析できる。
論文情報
- 掲載誌:
- npj Drug Discovery
- タイトル:
- Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design
- 著者:
- Masami Sako, Nobuaki Yasuo, Masakazu Sekijima
研究者プロフィール
酒向 正己 Masami Sako
東京科学大学 情報理工学院 情報工学系 博士後期課程学生
研究分野:AI創薬、マテリアルズインフォマティクス、機械学習
安尾 信明 Nobuaki Yasuo
東京科学大学 物質理工学院 特任准教授
研究分野:機械学習、AI創薬、ケモインフォマティクス
関嶋 政和 Masakazu Sekijima
東京科学大学 情報理工学院 情報工学系 准教授
研究分野:AI創薬、ケモインフォマティクス、マテリアルズインフォマティクス、機械学習