ポイント
- 亜鉛欠乏ストレスが、ヒストンアセチル基転移酵素KAT7の活性低下を介してH3K14のアセチル化(H3K14ac)を減少させ、遺伝子発現変化を引き起こす分子機構を解明
- H3K14acの減少が、亜鉛トランスポーターZIP10の発現を上昇させ、細胞内亜鉛量を回復する恒常性維持機構として機能することを明示
- 亜鉛欠乏に伴うH3K14ac低下が肝脂質蓄積を促進することを明らかにし、栄養状態と脂肪肝を結ぶ新たなエピゲノム制御基盤を提示
概要
東京科学大学(Science Tokyo) 総合研究院 高等研究府の藤澤貴央連携研究員、竹中哲プロジェクト研究員、一條秀憲特別栄誉教授らの研究チームは、亜鉛欠乏がヒストンH3の14番目のリジン残基のアセチル化(H3K14ac)を減少させることにより、遺伝子発現の変化を引き起こす分子機構を明らかにしました。
亜鉛は、生体における必須微量元素として健康の維持に重要であり、亜鉛欠乏はさまざまな疾患との関連が指摘されています。一方で、亜鉛欠乏状態がどのように感知され、どのようなストレス応答を誘導し、さらにどのように疾患形成へ寄与するのかについては、十分に解明されていませんでした。
今回、研究グループは、亜鉛欠乏ストレスによりH3K14acが減少することを発見し、その詳細な分子機構を明らかにしました。さらに、亜鉛欠乏によるH3K14acの減少が、細胞内の亜鉛恒常性の維持に寄与していることや、肝臓における脂肪の蓄積に関与することを見いだしました。
本研究は、亜鉛欠乏ストレスがエピゲノムシグナルへと変換され、生体内で機能する分子機構の一端を明らかにしたものです。亜鉛欠乏を伴う疾患に対する新たな予防・治療法の開発につながる可能性が期待されます。
本成果は、2月18日に「Nature Communications」誌に掲載されました。
背景
亜鉛は、多くのタンパク質の立体構造の維持や酵素活性に関わる必須微量元素であり、体内で亜鉛恒常性を保つことは健康の維持にとって非常に重要です。一方、亜鉛欠乏は、摂取不足・吸収障害・加齢など、さまざまな要因によって生じ得ます。1960年代にヒトにおける亜鉛欠乏症が報告されて以降、亜鉛の欠乏が皮膚障害・免疫機能低下・成長障害・がん・炎症性腸疾患・慢性腎臓病など、多様な疾患と関連することが示されてきました。しかし、亜鉛がどのような分子機構を通じてそれらの病態形成に関与しているのか、その全体像は十分に解明されていませんでした。
また、これまでの研究から、亜鉛欠乏ストレスが細胞の遺伝子発現変動を誘導することは知られていたものの、亜鉛欠乏がどのように細胞内で感知され、どのような仕組みで遺伝子発現を制御しているのかについては、不明な点が多く残されていました。遺伝子発現の制御には、ヒストンの翻訳後修飾などのエピゲノム制御が重要な役割を担います。ヒストン修飾は、"writer(付加酵素)"と"eraser(除去酵素)"のバランスによって制御されますが、これらの酵素群の中には亜鉛結合ドメインを持つものが複数存在し、細胞内の亜鉛量のバランスがヒストン修飾の動態を左右し得ることが示唆されています。
そこで本研究では、亜鉛欠乏ストレスによる遺伝子発現制御の分子機構について、ヒストン修飾に着目し、その生理学的および病態生理学的意義の解明を試みました。
研究成果
亜鉛欠乏による遺伝子発現変化の分子機構を解明するため、本研究では、遺伝子発現制御に重要な役割を担うことが知られているヒストン修飾に着目して研究を開始しました。まず、亜鉛欠乏ストレスによりヒストン修飾が変動するかどうかを検討したところ、ヒストンH3の14番目のリジン残基のアセチル化(H3K14ac)が特異的に減少することを見いだしました。
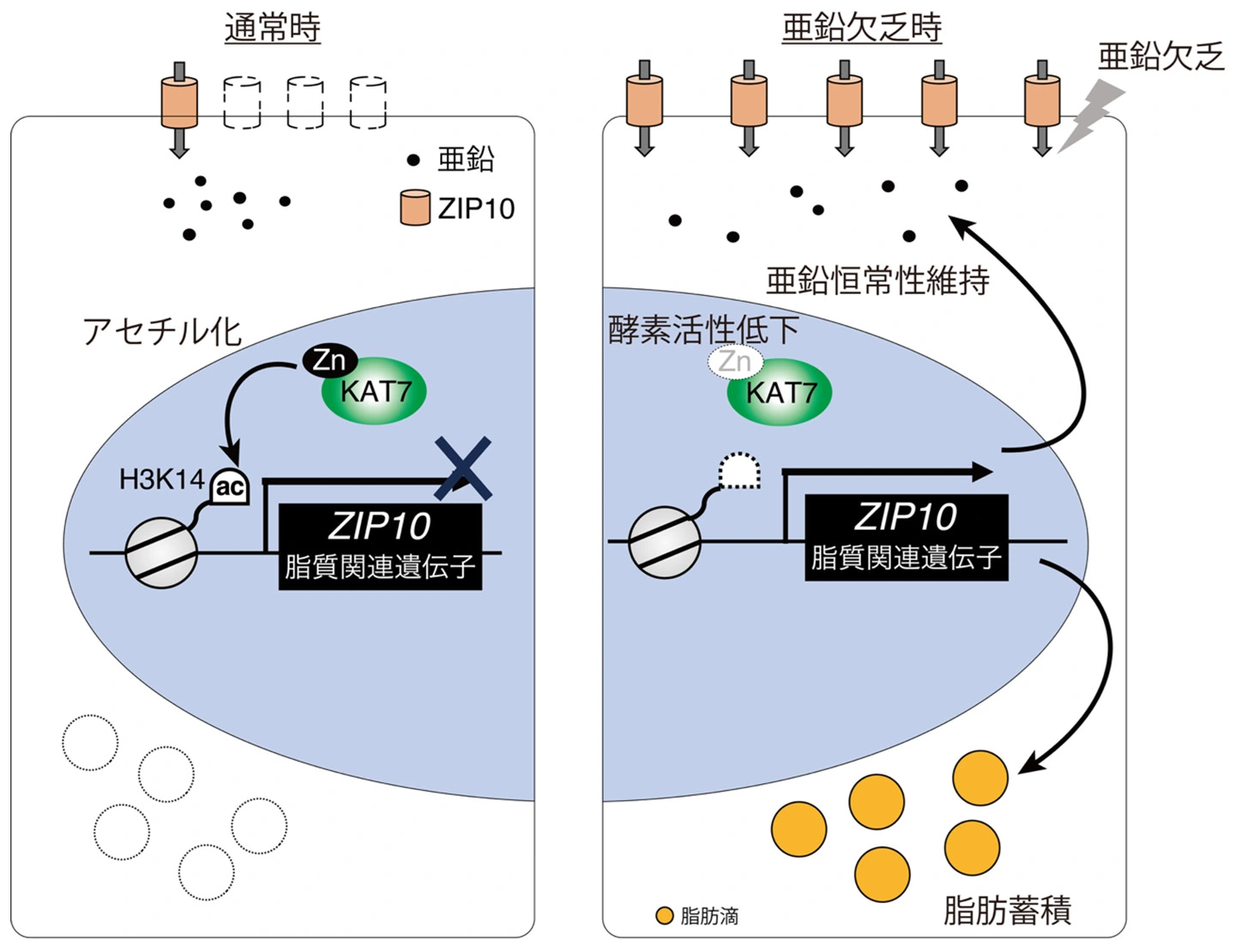
そこで、H3K14acが減少する分子機構の解析を進めた結果、ヒストンにアセチル基を付加するヒストンアセチル基転移酵素の1つであるKAT7が、亜鉛欠乏により活性を失うことを明らかにしました。また、KAT7の亜鉛配位ドメインが酵素活性の発揮に重要であることも示しました。これらの結果から、亜鉛欠乏によりKAT7が亜鉛を失うことで酵素活性が低下し、その結果H3K14acが減少することが示唆されました。
続いて、亜鉛欠乏によるH3K14ac低下の生理的意義を明らかにするため、亜鉛恒常性維持機構に着目して研究を行いました。その結果、細胞内へ亜鉛を輸送する亜鉛トランスポーターZIP10が、H3K14acの減少により発現上昇することを示しました。これにより、H3K14acの減少が、細胞内の亜鉛量を回復させる亜鉛恒常性維持機構として機能していることを明らかにしました。
さらに、H3K14ac低下の病態生理学的意義を検討するため、亜鉛欠乏を伴う疾患の探索を行いました。その結果、高脂肪食を与えたマウスの肝臓において亜鉛量が低下していることを見いだし、肝臓内の亜鉛量の低下が脂肪の蓄積を促進することを明らかにしました。また、マウスモデルを用いた解析により、亜鉛欠乏による脂肪の蓄積がH3K14acの減少によって誘発されることを示しました。
今後の展開
本研究では、亜鉛欠乏ストレスがKAT7–H3K14acによるエピゲノム制御を介して遺伝子発現を変化させ、亜鉛恒常性の維持や肝脂質の蓄積といった生理・病理過程に結び付くことを示しました。本成果は、栄養状態(亜鉛)と代謝病態(脂肪肝)をつなぐ分子基盤の理解を深めるものであり、今後、脂肪肝のリスク評価や介入戦略の開発に貢献することが期待されます。
付記
本研究は以下の研究助成金のもとに行われました。
- 文部科学省科学研究費助成事業(JP22K06610、JP22H04804、19H05771)
- 国立研究開発法人日本医療研究開発機構(JP17gm5010001、JP22gm0010009、JP24gm1710013)
- 科学技術振興機構ムーンショット型研究開発事業(JPMJMS2022-18)
- 公益信託タニタ健康体重基金
- 統計数理研究所 公募型共同利用(2024-ISMCRP-2013)
- 情報・システム研究機構 研究者交流促進プログラム
論文情報
- 掲載誌:
- Nature communications
- タイトル:
- Pathophysiological Significance of Impaired KAT7-Dependent Histone H3K14 Acetylation During Zinc Deficiency
- 著者:
- Takao Fujisawa, Satoshi Takenaka, Lila Maekawa, Motoyuki Ogawa, Toshiyuki Kowada, Toshitaka Matsui, Shin Mizukami, Yugo Kato, Michio Suzuki, Hisashi Noma, Isao Naguro, and Hidenori Ichijo
研究者プロフィール
藤澤 貴央 Takao Fujisawa
東京科学大学 総合研究院 高等研究府 細胞情報学研究室 連携研究員
研究分野:ストレス応答研究
竹中 哲 Satoshi Takenaka
東京科学大学 総合研究院 高等研究府 細胞情報学研究室 プロジェクト研究員
研究分野:ストレス応答研究
一條 秀憲 Hidenori Ichijo
東京科学大学 総合研究院 高等研究府 細胞情報学研究室 特別栄誉教授
研究分野:ストレス応答研究全般
関連リンク
東京科学大学 総合研究院 高等研究府 細胞情報学研究室
プロジェクト研究員 竹中 哲
東京科学大学 総合研究院 高等研究府 細胞情報学研究室
特別栄誉教授 一條 秀憲