ポイント
- 長年不明であった連続的ポリエーテル環化酵素反応を解明。
- 自然界で広く保存された戦略。
- 超柔軟な酵素が、ペアが存在するときに構造が形成される過程を直接的に観察。
概要
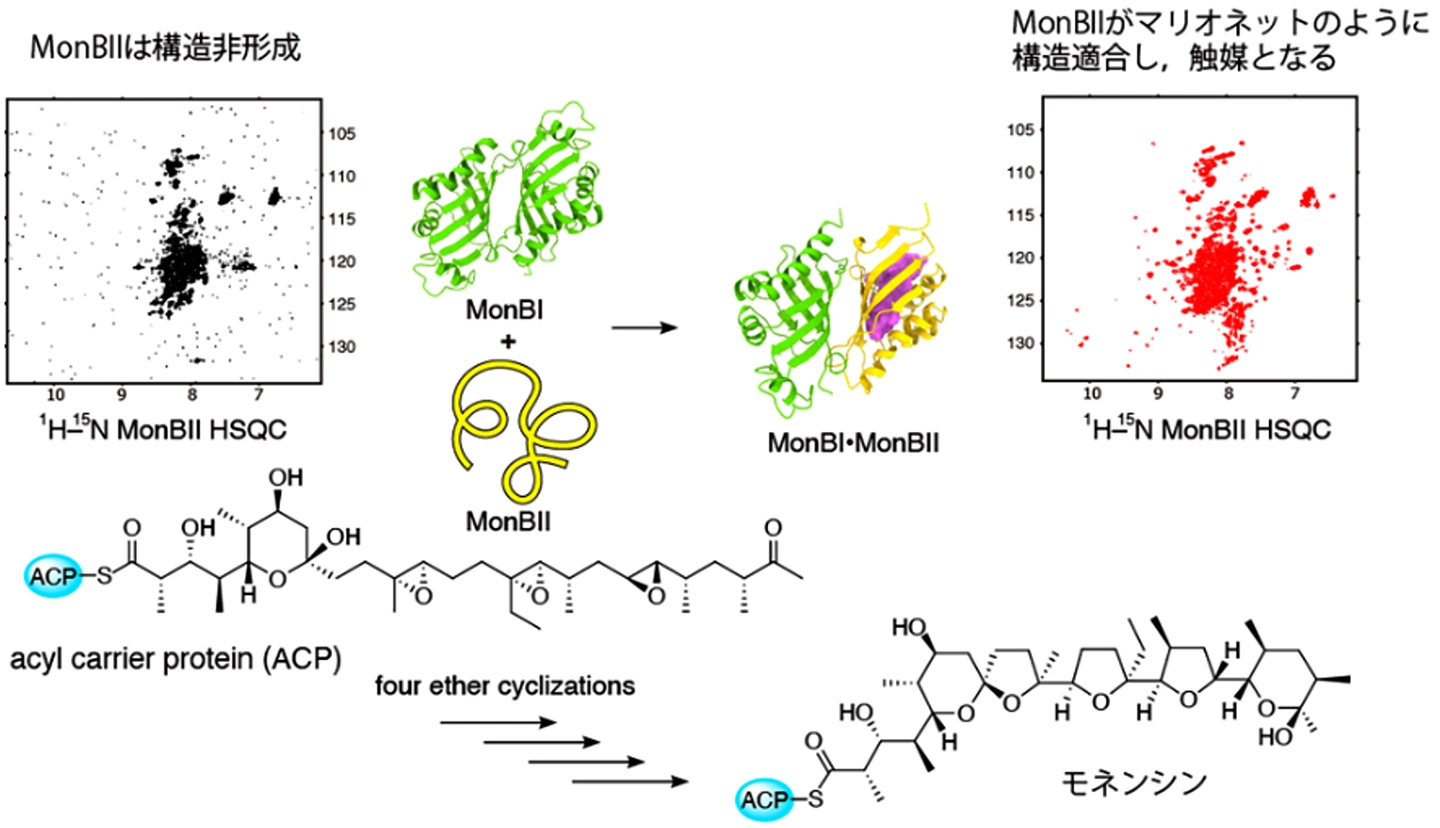
北海道大学大学院先端生命科学研究院の尾瀬農之教授、薮野奈々研究補佐員、久米田博之学術専門職、同大学の及川英秋名誉教授、同大学大学院理学研究院の尾崎太郎助教(研究当時、現・東北大学准教授)、東京科学大学理学院化学系の南篤志教授らの研究グループは、自然界に存在する天然化合物の主要な一群であるポリエーテル系天然物が作られる際の連続的環化反応を、特殊な工夫をして明らかにしました。ポリエーテルの代表的化合物モネンシンは抗生物質として利用されていますが、キーとなる生合成の過程で4回の連続的酵素環化反応が起こります。この反応はファスナーが閉じるように、端から順番に起こることが予測されていましたが、どういう蛋白質が具体的にどのように働くかは、分かっていませんでした。直前の基質は細長い化合物であり、酵素が収容するには大きなポケットが必要になります。近年流行しているAI(プログラム AlphaFold3 など)による構造・反応予測はできません。研究グループは、放線菌の遺伝子破壊、モデル基質[用語1]合成、結晶解析及び核磁気共鳴法[用語2]を組み合わせた構造評価、質量分析や種々の分析装置、分子動力学計算など、様々な角度から切り込むことにより、一つの蛋白質(MonBII)が4回の連続的酵素環化反応を触媒することを突き止めました。慎重にMonBIIを作製すると、溶液内では立体構造を取らない状態であることが分かりました。ここに相方であるMonBI蛋白質を添加すると、MonBIを鋳型として、MonBIIの構造形成が起こります。細胞の中でおこなわれている蛋白質の構造形成を、水溶液の中で再現できる例は極めて珍しいです。MonBIIは単独では構造非形成蛋白質ですが、構造非形成蛋白質が酵素として働く例もこれまでありませんでした。構造非形成蛋白質が必要な理由と合わせ、このタイプの蛋白質が広く存在することが明らかになり、化合物の合成や蛋白質の能力開発に対し、新たな展開の起点とすることができます。
なお、本研究成果は、日本時間2026年4月16日(木)公開の Nature Chemistry 誌にオンライン掲載されました。
背景
抗菌、シグナル伝達調節、免疫抑制作用など生理活性を持つ自然界に存在する化合物は天然物と称され、幾つかのグループに分けることができます。そのうち、ポリエーテル系天然物は、図1aのように、サイズの異なるエーテル環が多数連結した骨格を持っています。抗生物質として利用されてきましたが、さらに抗マラリア、抗がん作用にも期待が持たれています。他の天然物では発揮できない生理活性と特徴的な化学構造の相関から注目を集めてきました。また、生合成時の位置・立体選択性も含め、多くのエーテル環を持つポリエーテル型の天然物を生物がどのように作っているかという点において、有機化学を理解している生物の能力を明らかにし、有用化合物を手に入れるという視点からも、盛んに研究がおこなわれてきました。特に、1983年に、ケイン、セルマー及びウェストリーの3名の博士により提唱された説「ポリエン–ポリエポキシド仮説」は、ポリエーテルの作られ方を美しく説明するものでした。これは、1) ポリケタイド合成酵素[用語3]により生合成された鎖状ポリオレフィン前駆体に対し立体もコントロールしたエポキシ化が起こり、2) 生成したポリエポキシドに対し位置選択的なエーテル環化反応が次々に起こるというものです。「ポリエン-ポリエポキシド仮説」が非常に洗練された理論であることは、一つのエポキシド開環・エーテル環化反応が進行すると新しくヒドロキシ基が生じ、生じたヒドロキシ基が次のエポキシドに対して求核攻撃をおこなうという連鎖反応を可能にするという特徴にも顕れています(図1b)。
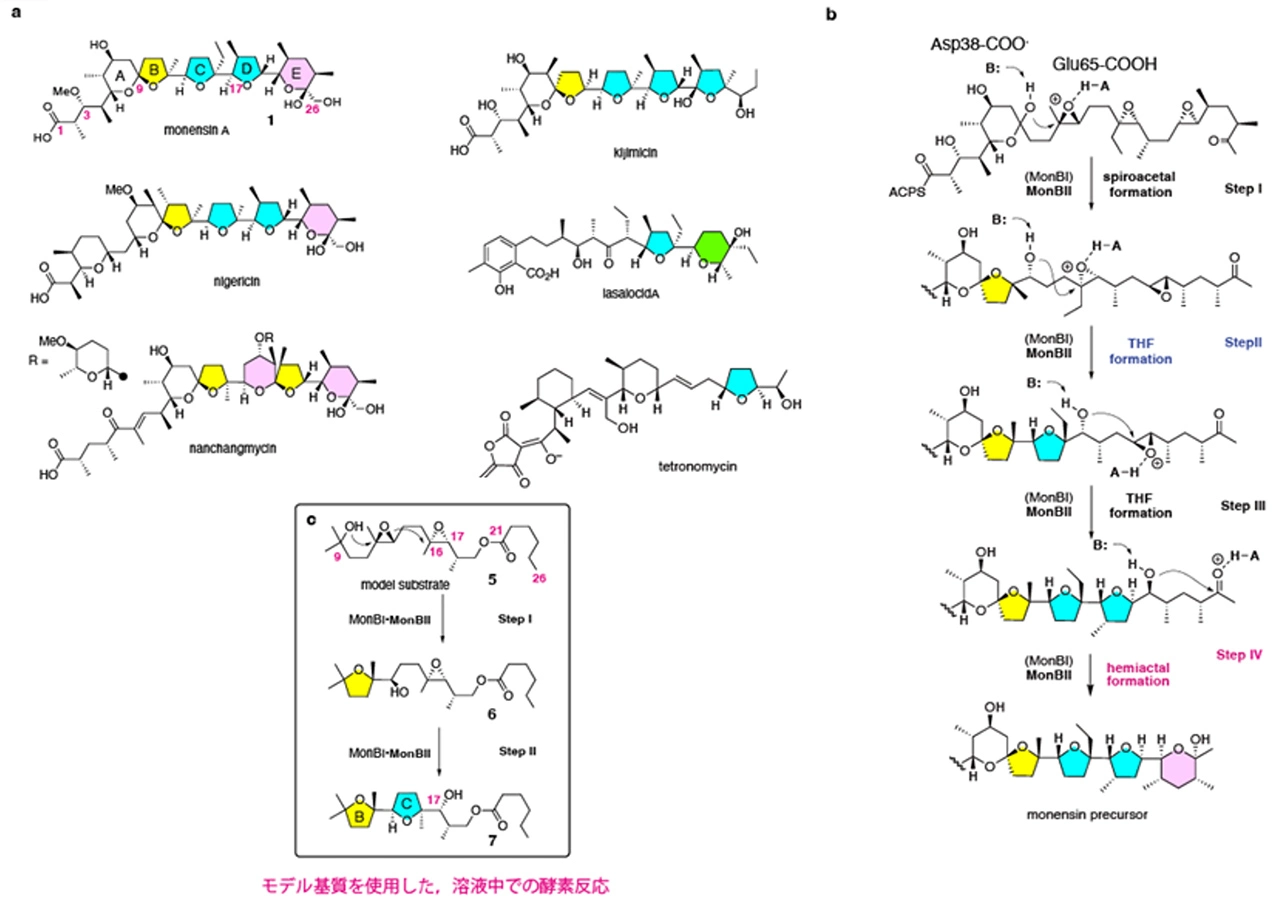
例えば、本研究で対象としたポリエーテル天然物モネンシンでは、ヒドロキシ基とエポキシド(及び1回のケトン)の間の求核反応が4回連続で起こることが、化合物の構造を見ると予測できていました(図1b)。ヒドロキシ基とエポキシド基の間で起こる反応が、エポキシド加水分解酵素のホモログ蛋白質(EPH)により触媒されることは、同じポリエーテル天然物であるラサロシドの研究により発表していました(2012年Nature 誌等)。さらにモネンシン研究において、研究グループは生産菌である放線菌の生合成遺伝子クラスター解析から、EPHとしてMonBIとMonBIIという二つの蛋白質がエポキシド開環・エーテル環化反応を触媒することを予測し、精製蛋白質及びモデル基質(図1c)合成から、MonBIIの酵素活性を2014年に報告しています(ACS Chem. Biol. 誌等)。その際の研究で生じた謎としては、MonBIは酵素活性を持たず、MonBIIに酵素活性があると考えられることの背景、及び、MonBIが存在しないとMonBIIが機能しないことは何故か、というものでした。
これまでのモデル基質を使用した研究では、(図1b)の反応の全貌を証明できないことや、類似蛋白質同士であるMonBIがMonBIIにどのように働きかけるか、環化反応が二つしかないラサロシド生合成経路では一般化できない、ポリエン–ポリエポキシド仮説における連鎖的環化反応はどのように進行するかを明らかにしたのが、本研究成果です。
研究成果
MonBIには、触媒反応に必要な要素(反応場としてのポケット、触媒残基となる二つのカルボキシ側鎖を持ったアミノ酸)が存在します。しかし、研究グループは、MonBIには一切触媒活性が無いという考えを持つに至りました。このことを証明するためにまず、モネンシンを生産する放線菌のMonBI遺伝子を破壊しました。破壊株にモネンシン生合成能が無いことを確認した上で、MonBI活性残基相当残基に変異を加えたΔmonBI + monBI E64A株を作製したところ、モネンシン生合成能が回復しました。このことは、MonBIの活性部位が使われず、MonBIIの活性部位だけを使って4回のエポキシド開環・エーテル環化反応が起こっていることが完全に証明できたことを意味します。
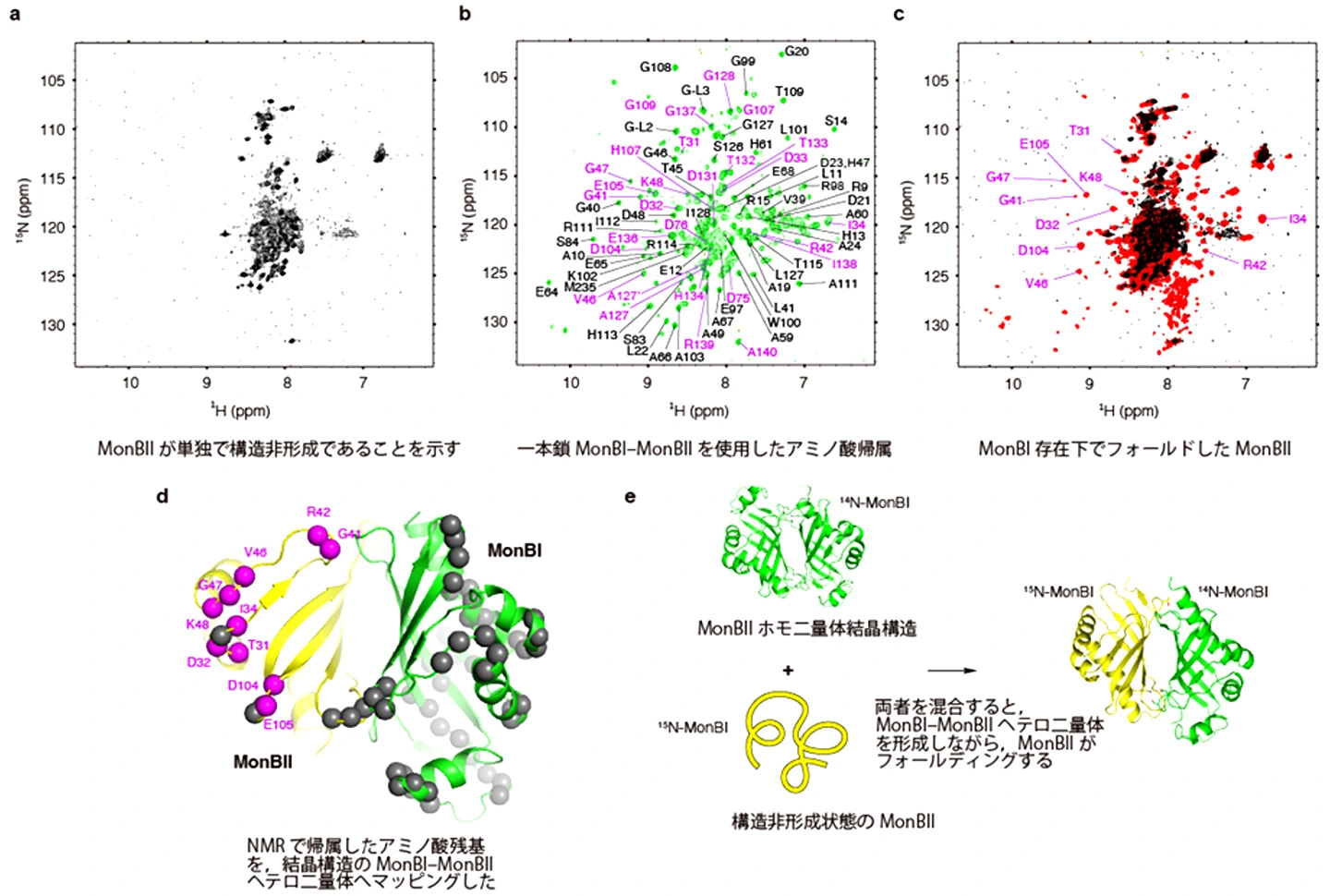
MonBIの活性部位は使われないですが、MonBIが存在しないとMonBIIに酵素活性が生まれません。何が起こっているかを知るために、MonBIとMonBIIを精製して、核磁気共鳴法(NMR法)によりMonBIIの性状を評価しました。MonBIIのみ2H、13C、15N原子に代えた蛋白質(ラベル体)を用いて測定したところ、MonBIIは単独では立体構造を取らない蛋白質(構造非形成蛋白質、IDP)であるものの、MonBIを添加すると、構造形成することが分かりました。すなわち、MonBIIはMonBIを鋳型として鋳造されるイメージなので、論文のタイトルをmouldable enzymeとしました(米語ではmoldable)。鋳型や足場、或いはシャペロン分子があって初めて立体構造を形成できる蛋白質が細胞の中に沢山存在することは知られていますが、MonBI/MonBIIのペアシステムが特殊なのは、両者が酷似する蛋白質であることと、細胞外に取り出して水溶液の中でMonBIIの構造が折れ畳まっていく様子を観測できることです(図2)。MonBIの介助により、MonBIIは大きなポケットを内部に作り出すことができ、長い出発物質を取り込むことができます。一般にIDPは単独で集合体をとりやすく、変化(へんげ)自在の蛋白質であるといわれていますが、MonBIIが様々な状態を取り得ることをNMRや質量分析など種々の方法で確認できました。構造解析に必要となる結晶を得るために、MonBIとMonBIIを結んだ人工一本鎖蛋白質を作りました。一本鎖MonBI–MonBIIの酵素活性は、単独のMonBIとMonBIIを混合したものよりやや低かったのです。すなわち、別々の蛋白質として存在し、出会ったときに構造形成をするという戦略が生物にとって有用であることが判明しました。
他のポリエーテル天然物の生合成経路とも比較しました。論文には、モネンシンと良く似た天然物であるキジマイシンの生合成遺伝子クラスターを同定したことも記載しています。EPHのアミノ酸配列の比較をおこなうと、ポリエーテル天然物プロトタイプと考えられるテトロノマイシンから、より複雑なポリエーテル生合成が可能になるように、EPHはMonBI型とMonBII型に進化した様子を見ることができます。AlphaFold3の通常の使用法では、MonBI型とMonBII型がヘテロ二量体を形成することを予測することはできませんが、それぞれのEPHの構造予測をおこなうと、MonBI型は分子内キャビティが小さく堅い構造、MonBII型は分子内キャビティがとても大きく、変化自在な構造であることがうかがえ、多くはMonBI型に酵素活性が無くMonBII型構造形成のための鋳型であることを予測できます(図3a)。ナンチャンマイシンのEPHは、MonBI型が活性残基相当のカルボキシ基を持たないことも、この考察を裏付けています。
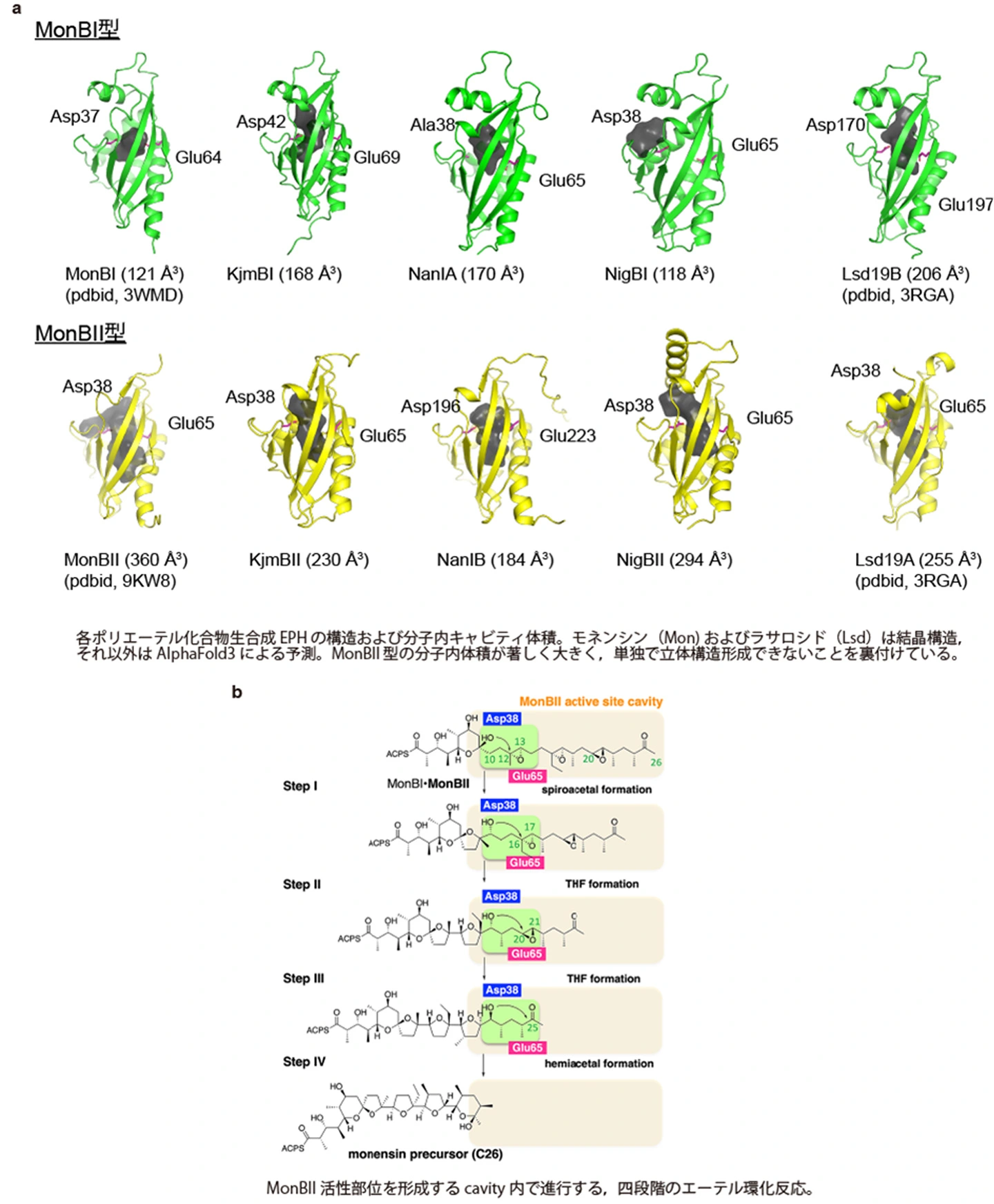
MonBII型が単独では構造非形成蛋白質であることは、論文中で記載した分子動力学計算の結果とも一致しています。モネンシン生合成の基質は長細く、最初の反応点(ヒドロキシ+エポキシド)を活性残基にセットするためには、奥深くまで挿入する必要があります(図3b)。この状態から、エポキシド開環・エーテル環化反応が進行する度に、少しずつ基質が引き抜かれていき、最後まで引き抜かれた状態が、モネンシンの基本構造となります。各反応の基質は、ステップ毎に立体化学や置換基が異なるものあるため、活性部位を柔らかくする必要が生じ、ペア型の戦略が必要だったのでしょう。なぜ、単に柔らかい構造であることだけでは不充分で、構造非形成蛋白質の性質を帯びるのかは、今後の研究も必要なところです。今までの結果を総合すると、MonBI–MonBII結晶構造で見たような状態で最初の基質を捕まえるわけではなく、MonBIIは一旦MonBIから離れて基質を捉えに行く投網のようなことをしていると考えています。
今後の展開
蛋白質構造生物学と呼ばれる研究領域に対するAIの貢献として、立体構造予測知能AlphaFoldはとても有名であり、基礎・応用を問わず各方面へ影響を与え、研究のやり方を根本的に変えるまでに至っています。しかし、AIによる構造予測が成功することは、構造形成される様子が明らかになったことではありません。あるアミノ酸配列があった場合、どういう順序で蛋白質の構造ができていくかは、依然謎のままです。MonBIIを使うことにより、蛋白質立体構造形成の経過を追跡できるため、本当の意味での蛋白質フォールディング問題に取り組むことが可能になり、その結果は再度AIにフィードバックできるため、「見かけだけでは無い蛋白質フォールディング問題」に迫ることができると考えています。本研究結果のように、ペアを組むことで機能を発揮する蛋白質が存在する情報を使い、新たなインプット情報を得たAIを使用することで、これまで見逃されていた反応を発見することに繋がります。具体例としては、抗がん剤候補サリノマイシンや、エンジイン系抗生物質の生合成遺伝子の中で見られる類似蛋白質が、ペアとなって働く可能性を追求できるようになります。
MonBII型EPHが構造非形成蛋白質でなければいけない理由は、蛋白質工学を進める上で重要になってくると考えています。語感から、「安定な蛋白質」とは堅固な蛋白質をイメージしがちですが、柔らかい蛋白質が(エネルギー的に)安定でいられる性質を利用し、新たな触媒や効率性を上げた酵素を設計することにつながることが考えられます。
付記
本研究は、文部科学省科学研究費補助金 学術変革領域研究(A)「予知生合成科学(JP25H01575、JP23H04533)」、学術変革領域研究(A)「潜在空間分子設計(JP24H01741)」、基盤研究(B)(JP23K23471)、挑戦的研究(萌芽)(JP22K19282)、新学術領域「生合成リデザイン(JP19H04634)」、北海道大学総合研究基盤連携センターオープンファシリティユニット、北海道大学先端NMRファシリティの支援を受けて行われました。
用語説明
- [用語1]
- モデル基質:自然界に存在する完全な基質ではなく、研究に着目した特徴を反映した疑似基質のこと。天然の基質では捉えられない中間体を解析する目的や、天然の基質を使用することが現実的ではない場合に用いられる。MonBIIの天然の基質は、アシルキャリア蛋白質(ACP)とチオエステル結合をしたトリエポキシド化合物であり、反応性が高いために解析に用いることが困難である。そのため、様々なモデル基質を合成し、反応解析に使用した(図1cなど)。
- [用語2]
- 核磁気共鳴法(NMR法):強力な磁場中に対象分子(この場合は蛋白質MonBII)を入れて、注目している原子核に由来する共鳴シグナルから、注目している原子の環境を観測する方法。MonBIIが構造非形成蛋白質であることは、注目している原子の運動性が高いことから判断できる。MonBIが存在した場合において運動性の高い原子が、特徴的な環境に移行する様子も捉えることができた。北海道大学先端NMRファシリティに設置されている、高性能800MHzのNMR装置を使用することで、本研究が可能となった。
- [用語3]
- ポリケタイド合成酵素(PKS) :生理活性を持つ天然物のうち、代表的な一群を形成するポリケタイドを生合成する酵素群。I型ーIII型に分類され、抗生物質や抗がん作用などを発揮する複雑な化合物骨格を生合成することができる。本研究で対象としているポリエーテル化合物は、放線菌の持つI型PKSによりポリケタイド骨格が作られた後、オレフィン部位がエポキシ化酵素によりエポキシ化され、EPHの基質となる。一連の生合成遺伝子クラスターから、生合成される化合物の構造が指定される。
論文情報
- 掲載誌:
- Nature Chemistry
- タイトル:
- A system of paired polyether epoxide hydrolases enables a mouldable enzyme for consecutive ring cyclization cascades(相方として鋳型をもちいた構造形成戦略により、ポリエーテル生合成連続環化反応が可能となる)
- 著者:
- 薮野奈々1、南篤志2(研究当時), 3、尾崎太郎2(研究当時)、大和田ゆうき1、澤田光平4、荒井彩花1、佐藤秀亮3、杉山葵1、田所高志4、相沢智康1、道仙卓也4、野間井智4、松丸尊紀4、Junyan Liu5、Tao Ye6、兒玉篤治7、内山進7, 8、Kowit Hengphasatporn9、重田育照9、齋尾智英2、前仲勝実4、姚閔1、久米田博之1、及川英秋2、尾瀬農之1
(1. 北海道大学大学院先端生命科学研究院、2. 北海道大学大学院理学研究院、3. 東京科学大学理学院化学系、4. 北海道大学大学院薬学研究院、5. Wuyi University、6. Ewha Womans University、7. 自然科学研究機構生命創成探究センター、8. 大阪大学大学院工学研究科、9. 筑波大学計算科学研究センター)
関連リンク
北海道大学
名誉教授 及川 英秋
- hoikmm1@icloud.com
- Tel
- 011-301-2332
東京科学大学 理学院 化学系
教授 南 篤志
- Tel
- 03-5734-2631
東京科学大学 総務企画部 広報課
- media@adm.isct.ac.jp
- Tel
- 03-5734-2975
- FAX
- 03-5734-3661